题目内容
15.已知反应X+Y=M+N为吸热反应,对这个反应的下列说法中正确的是( )| A. | X的能量一定低于M的,Y的能量一定低于N的 | |
| B. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| C. | 破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量 | |
| D. | 增加X的物质的量,该反应的化学反应速率一定加快 |
分析 反应X+Y=M+N为吸热反应,则X、Y的总能量小于M、N的总能量,吸热反应的反应条件不一定需要加热,且该反应中断裂化学键吸收的热量大于生成键释放的能量.
解答 解:A.由吸热反应,则X、Y的总能量小于M、N的总能量,但无法确定X与M、Y与N的能量高低,故A错误;
B.该反应为吸热反应,与反应条件无关,该反应可能需要加热,也可能不需要加热,故B错误;
C.该反应为吸热反应,则断裂化学键吸收的热量大于生成键释放的能量,故C正确;
D.若X为固体,增加X的物质的量,该反应的化学反应速率不变,故D错误;
故选C.
点评 本题考查吸热反应,明确化学反应中能量变化的实质及利用反应物、生成物的总能量的相对大小判断吸热反应、放热反应的方法即可解答,题目难度不大.

练习册系列答案
相关题目
10.煤和石油与生活密切相关,下列有关煤和石油的综合利用中,属于物理变化的是( )
| A. | 煤的干馏 | B. | 煤的气化和液化 | ||
| C. | 石油的分馏 | D. | 石油的裂化和裂解 |
6.由于发生化学反应而使溴水褪色的一组物质是( )
①甲苯 ②聚乙烯 ③四氯化碳 ④2-丁炔 ⑤(CH3)2C=CHCH3.
①甲苯 ②聚乙烯 ③四氯化碳 ④2-丁炔 ⑤(CH3)2C=CHCH3.
| A. | ①④ | B. | ②④⑤ | C. | ④⑤ | D. | ①③④⑤ |
3.下列说法正确的是( )
| A. | 能够使品红试液褪色的气体一定是SO2 | |
| B. | 常温下,铁、铝不与浓硫酸反应,因此可以用铁、铝容器贮存运输浓硫酸 | |
| C. | 硝酸铵受热易分解爆炸,实验室常加热氯化铵与氢氧化钙的混合物制备氨气 | |
| D. | 一种元素可能有多种氧化物,但同种化合价只对应一种氧化物 |
10.等质量的下列有机物完全燃烧时,耗氧量最大的是( )
| A. | 苯 | B. | 乙烯 | C. | 乙烷 | D. | 甲烷 |
20.同一周期的X、Y、Z三种元素,其最高价氧化物对应水化物的酸性强弱顺序为:HZO4>H2YO4>H3XO4,则下列判断正确的是( )
| A. | 单质的氧化性为:Z>Y>X | B. | 非金属性:X>Y>Z | ||
| C. | 气态氢化物的稳定性:XH3>H2Y>HZ | D. | 原子半径:Z>Y>X |
7.某课外小组同学通过实验发现钾和钠的化学性质相似.下列解释最合理的是( )
| A. | 都属于金属元素 | B. | 原子半径相差不大 | ||
| C. | 原子的电子层数相接近 | D. | 原子的最外层电子数相同 |
5.门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确.根据元素周期律,下列有关X性质的描述中错误的是( )
| A. | X单质不易与水反应 | B. | XO2可被碳或氢气还原为X | ||
| C. | XH4的稳定性比SiH4的高 | D. | XCl4的沸点比SiCl4的高 |
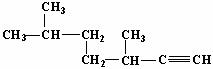 的名称为3,6-二甲基-1-庚炔;
的名称为3,6-二甲基-1-庚炔;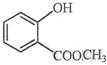 中含氧官能团的名称为羟基、酯基.
中含氧官能团的名称为羟基、酯基.