题目内容
20.写出下列反应的化学方程式.(1)碳酸钠与盐酸反应NaHCO3+HCl=NaCl+H2O+CO2↑..
(2)铝与氧化铁的铝热反应(注明条件)2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe.
分析 (1)碳酸钠与盐酸发生复分解反应生成氯化钠、水、二氧化碳;
(2)铝比铁活泼还原性强于铁,氧化铁与铝反应生成铁与氧化铝.
解答 解:(1)盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑,
故答案为:NaHCO3+HCl=NaCl+H2O+CO2↑;
(2)氧化铁与铝反应生成铁与氧化铝,化学方程式:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,
故答案为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe.
点评 本题考查反应方程式的书写,为高频考点,侧重考查学生根据反应原理书写化学方程式的能力,把握发生的化学反应书写方法为解答的关键,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.已知 I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为Cl-<H2O2<Fe2+<I-<SO2,则下列反应不能发生的是( )
| A. | 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ | B. | I2+SO2+2H2O=H2SO4+2HI | ||
| C. | 2Fe3++2I-=2Fe2++I2 | D. | H2O2+H2SO4=SO2+O2+2H2O |
8.现有部分短周期元素的性质或原子结构如表:
(1)写出元素X电子排布式1s22s22p4.
(2)Z原子共有7种运动状态不同的电子.
(3)写出Z元素形成的单质的结构式:N≡N.
(4)元素T与氯元素相比,非金属性较强的是F(用元素符号表示),下列表述 中能证明这一事实的是C
A、常温下氯气的颜色比T单质的颜色深
B、T的单质通入氯化钠水溶液不能置换出氯气
C、氯与T形成的化合物中氯元素呈正价态
(5)探寻物质的性质差异性是学习的重要方法之-.T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是Al(填化学式),理由铝是金属单质,其它的是非金属单质.
(6)T与Z形成的化合物含有的化学键类型共价键.
| 元素编号 | 元素性质或原子结构 |
| T | 所有元素中电负性最大的元素 |
| X | L层p电子数比s电子数多2个 |
| Y | 其最高价氧化物呈两性 |
| Z | L层有三个未成对电子 |
(2)Z原子共有7种运动状态不同的电子.
(3)写出Z元素形成的单质的结构式:N≡N.
(4)元素T与氯元素相比,非金属性较强的是F(用元素符号表示),下列表述 中能证明这一事实的是C
A、常温下氯气的颜色比T单质的颜色深
B、T的单质通入氯化钠水溶液不能置换出氯气
C、氯与T形成的化合物中氯元素呈正价态
(5)探寻物质的性质差异性是学习的重要方法之-.T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是Al(填化学式),理由铝是金属单质,其它的是非金属单质.
(6)T与Z形成的化合物含有的化学键类型共价键.
15.下列物质的水溶液,滴加稀硫酸或氯化镁溶液时,均有白色沉淀生成的是( )
| A. | BaCl2 | B. | NaHCO3 | C. | Ba(OH)2 | D. | NaOH |
10.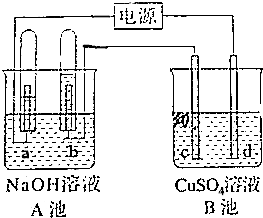 如图所示,A池用石墨电极电解pH=13的Na0H溶液100mL,B池为模拟电解精炼铜的装置,其中c电极为纯铜,d电极为粗铜(含有杂质Fe、Ag),溶液是足量CuSO4溶液,通电一段时间后停止电解,A池a极上产生的气体在标准状况下为2.24L,则下列说法正确的是( )
如图所示,A池用石墨电极电解pH=13的Na0H溶液100mL,B池为模拟电解精炼铜的装置,其中c电极为纯铜,d电极为粗铜(含有杂质Fe、Ag),溶液是足量CuSO4溶液,通电一段时间后停止电解,A池a极上产生的气体在标准状况下为2.24L,则下列说法正确的是( )
 如图所示,A池用石墨电极电解pH=13的Na0H溶液100mL,B池为模拟电解精炼铜的装置,其中c电极为纯铜,d电极为粗铜(含有杂质Fe、Ag),溶液是足量CuSO4溶液,通电一段时间后停止电解,A池a极上产生的气体在标准状况下为2.24L,则下列说法正确的是( )
如图所示,A池用石墨电极电解pH=13的Na0H溶液100mL,B池为模拟电解精炼铜的装置,其中c电极为纯铜,d电极为粗铜(含有杂质Fe、Ag),溶液是足量CuSO4溶液,通电一段时间后停止电解,A池a极上产生的气体在标准状况下为2.24L,则下列说法正确的是( )| A. | d电极质量一定减少6.4g | B. | c电极质量一定增加6.4g | ||
| C. | A池pH不变 | D. | A池溶液质量减少3.6g |