题目内容
下列各表述与示意图一致的是( )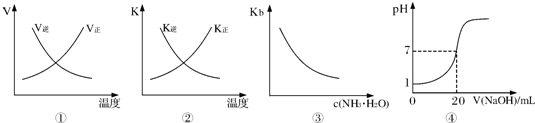

| A、图①表示反应N2(g)+O2(g)?2NO(g)△H>0正、逆反应的速率随温度的变化 | B、图②表示反应N2(g)+3H2(g)?2NH3(g)△H<0正、逆反应的平衡常数随温度的变化 | C、图③表示氨水的电离平衡常数随氨水浓度c(NH3?H2O)的变化 | D、图④表示25℃时,用0.1mol?L-1NaOH溶液滴定20mL 0.lmol?L-1盐酸,溶液的pH随加入碱体积的变化 |
分析:A、该反应为吸热反应,升高温度后,正逆反应速率都增大,而图象中达到平衡后升高温度,逆反应速率减小是错误的;
B、对应放热反应,达到平衡后温度升高,平衡向着逆向移动,逆反应的平衡常数应该增大,正反应平衡常数减小,图象与实际反应不相符;
C、电离平衡常数只与温度有关,温度不变,平衡常数不变,图象与图象中平衡常数随着浓度的增大而增大是错误的;
D、0.lmol?L-1盐酸的pH为1,二者都是一元强酸、强碱,浓度相同,所以当加入20mL氢氧化钠时恰好反应.
B、对应放热反应,达到平衡后温度升高,平衡向着逆向移动,逆反应的平衡常数应该增大,正反应平衡常数减小,图象与实际反应不相符;
C、电离平衡常数只与温度有关,温度不变,平衡常数不变,图象与图象中平衡常数随着浓度的增大而增大是错误的;
D、0.lmol?L-1盐酸的pH为1,二者都是一元强酸、强碱,浓度相同,所以当加入20mL氢氧化钠时恰好反应.
解答:解:A、该反应为吸热反应,温度升高,正逆反应速率都增大,平衡向着正向移动,所以正反应速率大于逆反应速率,而图象中达到平衡后升高温度,逆反应速率减小是错误的,逆反应速率也应该增大,故A错误;
B、该反应为放热反应,升高温度后平衡向着逆向移动,所以逆反应的平衡常数增大,正反应的平衡常数减小,而图象中达到平衡后升高温度,逆反应的平衡常数减小、正反应的平衡常数增大与实际不相符,故B错误;
C、氨水的电离平衡常数与浓度没有关系,只受温度的影响,所以温度不变,电离平衡常数不变,而图象中平衡常数随着氨水的浓度增大而减小是错误的,故C错误;
D、25℃时,用0.1mol?L-1NaOH溶液滴定20mL 0.lmol?L-1盐酸,滴定前盐酸的pH=1,随着氢氧化钠体积不断增大,溶液的pH逐渐增大,当加入20mL氢氧化钠溶液时,二者恰好反应,溶液的pH=7,该图象符合反应实际,故D正确;
故选D.
B、该反应为放热反应,升高温度后平衡向着逆向移动,所以逆反应的平衡常数增大,正反应的平衡常数减小,而图象中达到平衡后升高温度,逆反应的平衡常数减小、正反应的平衡常数增大与实际不相符,故B错误;
C、氨水的电离平衡常数与浓度没有关系,只受温度的影响,所以温度不变,电离平衡常数不变,而图象中平衡常数随着氨水的浓度增大而减小是错误的,故C错误;
D、25℃时,用0.1mol?L-1NaOH溶液滴定20mL 0.lmol?L-1盐酸,滴定前盐酸的pH=1,随着氢氧化钠体积不断增大,溶液的pH逐渐增大,当加入20mL氢氧化钠溶液时,二者恰好反应,溶液的pH=7,该图象符合反应实际,故D正确;
故选D.
点评:本题考查图象分析,涉及铝化合物性质、碳酸盐性质、中和滴定、可逆反应等,难度中等,清楚反应过程与可逆反应的特点是关键,注意图象中量的关系.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
室温时,下列各表述与示意图一致的是( )
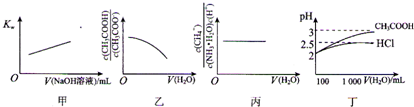

| A、图甲表示在纯水中加入0.01 moL?L-1 NaOH溶液,Kw与NaOH溶液体积变化关系 | ||
B、图乙表示将1 mol?L-1 CH3COONa溶液加水稀释,溶液中
| ||
C、图丙表示0.1mol?L-1 NH3?H2O加水稀释,溶液中
| ||
| D、图丁表示100 mL pH=2的HCl和CH3COOH加水稀释到1000mL时pH变化与水的体积的变化关系 |


