题目内容
下列关于物质的保存不正确的是( )
| A、AgNO3溶液应保存在棕色瓶中 |
| B、氯水保存在无色广口瓶中 |
| C、液氯可以保存在干燥的钢瓶中 |
| D、漂白粉可露置于空气中保存 |
考点:氯气的化学性质,氯、溴、碘及其化合物的综合应用,化学试剂的存放
专题:化学实验基本操作
分析:根据物质的性质选择保存方法,一般来说,易与空气中氧气、水、二氧化碳反应的物质应隔绝空气保存,见光易分解的物质应避光保存,加热易分解的物质应低温保存,易挥发的物质应密闭保存,结合物质的性质解答该题.
解答:
解:A.硝酸银见光易分解,应放在棕色瓶中避光保存,故A正确;
B.氯水中含有次氯酸,次氯酸不稳定,见光易分解,应放在棕色瓶中避光保存,故B错误;
C.液氯与干燥的钢瓶不反应,可用钢瓶保存,故C正确;
D.漂白粉的有效成分为次氯酸钙,次氯酸钙可与空气的水、二氧化碳反应生成不稳定的次氯酸,应隔绝空气保存,故D错误.
故选BD.
B.氯水中含有次氯酸,次氯酸不稳定,见光易分解,应放在棕色瓶中避光保存,故B错误;
C.液氯与干燥的钢瓶不反应,可用钢瓶保存,故C正确;
D.漂白粉的有效成分为次氯酸钙,次氯酸钙可与空气的水、二氧化碳反应生成不稳定的次氯酸,应隔绝空气保存,故D错误.
故选BD.
点评:本题考查了物质的存放,为高频考点,侧重于元素化合物知识的考查,明确物质的性质是解本题关键,根据物质的性质来分析解答,难度不大.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
活性炭可除水中氯气,反应为2Cl2+2H2O+C═4HCl+CO2,若水中Cl2浓度为4.0×10-6 mol/L,则每消耗96g活性炭,可处理上述水的体积是( )
| A、188.3 L |
| B、4.0×1010L |
| C、4.0×106L |
| D、8.0×106 L |
关于下列各装置图的叙述不正确的是( )
A、 用装置精炼铜,a极为粗铜,b为精铜,电解质溶液为CuSO4溶液 |
B、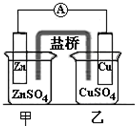 装置的盐桥中KCl的Cl-移向甲烧杯 |
C、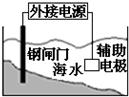 装置中钢闸门应与外接电源的正极相连获得保护 |
D、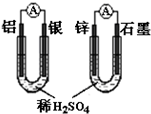 两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同 |
下列说法正确的是( )
| A、煤经处理变为气体燃料的过程属于物理变化 |
| B、淀粉、油脂和蛋白质都是高分子化合物 |
| C、乙烯和乙醇均可使酸性KMnO4溶液褪色 |
| D、乙酸乙酯和植物油均可水解生成乙醇 |
下列物质①过滤后的天然水 ②变浑浊的石灰水 ③石蕊试液 ④牛奶 ⑤盐酸 ⑥碘酒,其中属于溶液的是( )
| A、①③ | B、②④ |
| C、③⑤⑥ | D、①③⑤⑥ |
等质量的氢气在足量的氧气中燃烧,生成水蒸气时放出热量Q1,生成液态水时放出热Q2,则Q1与Q2的关系是( )
| A、Q1>Q2 |
| B、Q1<Q2 |
| C、Q1=Q2 |
| D、无法确定 |
下列可用相同的方法除去混有的杂质的是( )
| A、淀粉溶液中混有少量NaCl杂质;氯化钠溶液中混有少量Na2CO3杂质 |
| B、Fe(OH)3胶体中混有少量盐酸;淀粉溶液中混有少量KI |
| C、Na2CO3中混有少量NaHCO3;NaHCO3中混有少量Na2CO3 |
| D、铁粉中混有少量硫粉;碘中混有少量NaCl |
钠多以资源丰富的NaCl为原料来制备,下列方法中能够制备出金属钠的是( )
| A、加热NaCl晶体 |
| B、用金属钾置换出NaCl溶液中Na+ |
| C、电解NaCl溶液 |
| D、电解熔融的NaCl |