题目内容
下列操作中导致中和滴定的测量值偏小的是……( )
①锥形瓶用蒸馏水冲洗后,再用待测液润洗2-3次;②滴定开始时,滴定管尖嘴有气泡,滴定过程中气泡消失;③滴定前读数时仰视,滴定后读数平视;④摇动锥形瓶时,瓶中有少量液体溅出;⑤滴定时,锥形瓶中加入少量蒸馏水,稀释待测液。
①锥形瓶用蒸馏水冲洗后,再用待测液润洗2-3次;②滴定开始时,滴定管尖嘴有气泡,滴定过程中气泡消失;③滴定前读数时仰视,滴定后读数平视;④摇动锥形瓶时,瓶中有少量液体溅出;⑤滴定时,锥形瓶中加入少量蒸馏水,稀释待测液。
| A.只有③ | B.④和⑤ | C.①②和③ | D.③和④ |
D
①偏高;②偏高;③偏低;④偏低;⑤无影响。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
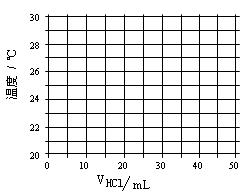
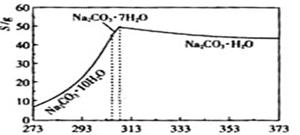
 等杂质,提纯工艺路线如下:
等杂质,提纯工艺路线如下: