题目内容
1.下列各组粒子中,互为同位素的是( )| A. | H T | B. | O2 O3 | C. | 红磷 白磷 | D. | H2 D2 |
分析 质子数相同中子数不同的原子互称同位素.互为同位素原子具有以下特征:
质子数相同、化学性质相同、在周期表中的位置相同;
中子数不同、质量数不同、物理性质不同;
研究对象为原子.
解答 解:A.H、T是氢元素的不同核素,互为同位素,故A正确;
B.O2、O3都是由氧元素形成的结构不同的单质,互为同素异形体,故B错误;
C.红磷、白磷都是由磷元素形成的结构不同的单质,互为同素异形体,故C错误;
D.H2、D2都是由氢元素组成的,不同氢气分子,结构相同,为同一物质,故D错误.
故选A.
点评 本题以同位素为载体,考查化学“五同”比较,难度不大,注意把握概念的理解,H2、D2都是由氢元素组成的,不同氢气分子,但结构相同,为同一物质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列各组元素的性质递变情况错误的是( )
| A. | Li、C、O原子最外层电子数依次增加 | B. | P、S、Cl元素最高正化合价依次升高 | ||
| C. | N、O、F原子半径依次增大 | D. | Li、Na、K的金属性依次增强 |
9.反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在2L的密闭容器中进行,1min后,NH3减少了0.12mol,则平均每秒钟浓度变化正确的是( )
| A. | NO:0.06mol•L-1 | B. | H2O:0.002mol•L-1 | ||
| C. | NH3:0.002mol•L-1 | D. | O2:0.00125mol•L-1 |
16.下表列出了①~⑨九种元素在周期表中的位置.请回答(用化学用语):
(1)在这些元素中,最活泼的金属元素是K;最活泼非金属元素是O;最不活泼的元素是Ar.
(2)这些元素的最高价氧化物对应的水化物中,酸性最强的化合物的分子式是HClO4;碱性最强的化合物的电子式 ;能形成两性氢氧化物的元素是Al.
;能形成两性氢氧化物的元素是Al.
(3)①、②、③三种元素的原子半径由大到小的顺序依次为K>Na>Mg.
(4)⑥元素的氢化物是H2O,该氢化物在常温下与②发生反应的化学方程式为2K+2H2O=2KOH+H2↑,所得溶液的pH> 7.
(5)用电子式表示①和⑧元素形成化合物的过程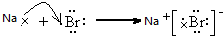 .
.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑨ | |||
| 4 | ② | ⑧ |
(2)这些元素的最高价氧化物对应的水化物中,酸性最强的化合物的分子式是HClO4;碱性最强的化合物的电子式
 ;能形成两性氢氧化物的元素是Al.
;能形成两性氢氧化物的元素是Al.(3)①、②、③三种元素的原子半径由大到小的顺序依次为K>Na>Mg.
(4)⑥元素的氢化物是H2O,该氢化物在常温下与②发生反应的化学方程式为2K+2H2O=2KOH+H2↑,所得溶液的pH> 7.
(5)用电子式表示①和⑧元素形成化合物的过程
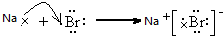 .
.
6.现有下列短周期元素性质的数据:
试回答下列问题:
(1)元素③在周期表中的位置是第二周期第ⅠA族;元素①②④⑦的气态氢化物中最稳定的是H2O(填化学式);
(2)上述元素形成的单核离子中半径最大的是P3-,半径最小的是Li+;
(3)元素①与元素⑥按照原子个数比为1:1形成的化合物与水反应的化学反应方程式2Na2O2+2H2O═4NaOH+O2↑;
(4)元素⑤形成的单质加入到元素②的氢化物的水溶液中,反应生成两种强酸的离子方程式4Cl2+H2S+4H2O═10H++8Cl-+SO42-.
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或 最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)元素③在周期表中的位置是第二周期第ⅠA族;元素①②④⑦的气态氢化物中最稳定的是H2O(填化学式);
(2)上述元素形成的单核离子中半径最大的是P3-,半径最小的是Li+;
(3)元素①与元素⑥按照原子个数比为1:1形成的化合物与水反应的化学反应方程式2Na2O2+2H2O═4NaOH+O2↑;
(4)元素⑤形成的单质加入到元素②的氢化物的水溶液中,反应生成两种强酸的离子方程式4Cl2+H2S+4H2O═10H++8Cl-+SO42-.
5.下列物质的主要成分不正确的是( )
| A. | 赤铁矿:Fe2O3 | B. | 硫铁矿:FeS | ||
| C. | 玛瑙:SiO2 | D. | 芒硝:Na2SO4•10H2O |
6.下列各组物质:①Cu和硝酸 ②Cu和氯化铁溶液③Zn和硫酸④Fe和盐酸由于浓度不同而发生不同反应的是( )
| A. | ①③ | B. | ③④ | C. | ①② | D. | ①③④ |
 乙
乙 丙
丙

 )
)