题目内容
【题目】水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
(1)Shibata曾做过下列实验:①使纯H2缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴(Co),平衡后气体中H2的物质的量分数为0.0250。
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192。
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO_________H2(填“大于”或“小于”)。
(2)721 ℃时,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应,则平衡时体系中H2的物质的量分数为_________(填标号)。
A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50
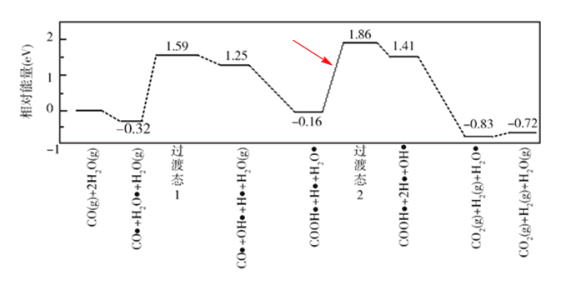
(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用![]() 标注。
标注。

可知水煤气变换的ΔH________0(填“大于”“等于”或“小于”),该历程中最大能垒(活化能)E正=_________eV,写出该步骤的化学方程式_______________________。
(4)Shoichi研究了467 ℃、489 ℃时水煤气变换中CO和H2分压随时间变化关系(如下图所示),催化剂为氧化铁,实验初始时体系中的PH2O和PCO相等、PCO2和PH2相等。

计算曲线a的反应在30~90 min内的平均速率![]() (a)=___________kPa·min1。467 ℃时PH2和PCO随时间变化关系的曲线分别是___________、___________。489 ℃时PH2和PCO随时间变化关系的曲线分别是___________、___________。
(a)=___________kPa·min1。467 ℃时PH2和PCO随时间变化关系的曲线分别是___________、___________。489 ℃时PH2和PCO随时间变化关系的曲线分别是___________、___________。
【答案】大于 C 小于 2.02 COOH![]() +H
+H![]() +H2O
+H2O![]() =COOH
=COOH![]() +2H
+2H![]() +OH
+OH![]() 或H2O
或H2O![]() =H
=H![]() +OH
+OH![]() 0.0047 b c a d
0.0047 b c a d
【解析】
(1)由H2、CO与CoO反应后其气体物质的量分数判断二者的倾向大小;
(2)根据三段式以及CO与H2的倾向大小关系综合判断;
(3)根据反应物与生成物的相对能量差大小进行比较判断;根据反应物达到活化状态所需能量为活化能以及相对能量差值大小计算并比较最大能垒;根据最大能垒对应的反应历程对应的物质写出方程式;
(4)根据图中曲线a在30~90 min内分压变化量计算平均反应速率;先根据CO与H2的倾向大小关系判断CO与H2的含量范围,然后根据温度变化对化学平衡的影响判断出在不同温度下曲线对应的物质。
(1)H2还原氧化钴的方程式为:H2(g)+CoO(s)![]() Co(s)+H2O(g);CO还原氧化钴的方程式为:CO(g)+CoO(s)
Co(s)+H2O(g);CO还原氧化钴的方程式为:CO(g)+CoO(s)![]() Co(s)+CO2(g),平衡时H2还原体系中H2的物质的量分数(
Co(s)+CO2(g),平衡时H2还原体系中H2的物质的量分数(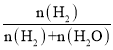 )高于CO还原体系中CO的物质的量分数(
)高于CO还原体系中CO的物质的量分数(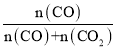 ),故还原CoO(s)为Co(s)的倾向是CO大于H2;
),故还原CoO(s)为Co(s)的倾向是CO大于H2;
(2)721 ℃时,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,可设其物质的量为1mol,则
CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
起始(mol) 1 1 0 0
转化(mol) x x x x
平衡(mol) 1-x 1-x x x
则平衡时体系中H2的物质的量分数=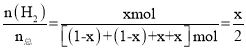 ,因该反应为可逆反应,故x<1,可假设二者的还原倾向相等,则x=0.5,由(1)可知CO的还原倾向大于H2,所以CO更易转化为H2,故x>0.5,由此可判断最终平衡时体系中H2的物质的量分数介于0.25~0.50,故答案为C;
,因该反应为可逆反应,故x<1,可假设二者的还原倾向相等,则x=0.5,由(1)可知CO的还原倾向大于H2,所以CO更易转化为H2,故x>0.5,由此可判断最终平衡时体系中H2的物质的量分数介于0.25~0.50,故答案为C;
(3)根据水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]并结合水煤气变换的反应历程相对能量可知,CO(g)+H2O(g)的能量(-0.32eV)高于CO2(g)+H2(g)的能量(-0.83eV),故水煤气变换的ΔH小于0;活化能即反应物状态达到活化状态所需能量,根据变换历程的相对能量可知,最大差值为:
(4)由图可知,30~90 min内a曲线对应物质的分压变化量Δp=(4.08-3.80)kPa=0.28 kPa,故曲线a的反应在30~90 min内的平均速率![]() (a)=
(a)=![]() =0.0047 kPa·min1;由(2)中分析得出H2的物质的量分数介于0.25~0.5,CO的物质的量分数介于0~0.25,即H2的分压始终高于CO的分压,据此可将图分成两部分:
=0.0047 kPa·min1;由(2)中分析得出H2的物质的量分数介于0.25~0.5,CO的物质的量分数介于0~0.25,即H2的分压始终高于CO的分压,据此可将图分成两部分:
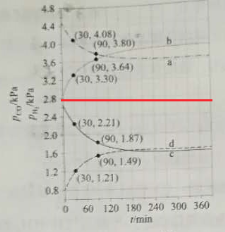
由此可知,a、b表示的是H2的分压,c、d表示的是CO的分压,该反应为放热反应,故升高温度,平衡逆向移动,CO分压增加,H2分压降低,故467 ℃时PH2和PCO随时间变化关系的曲线分别是b、c;489 ℃时PH2和PCO随时间变化关系的曲线分别是a、d。

 备战中考寒假系列答案
备战中考寒假系列答案