题目内容
【题目】下列说法正确的是( )
A. c(H+)>c(OH-)的溶液一定显酸性
B. 常温下,pH=6的溶液一定是酸溶液
C. 电解稀硫酸或氢氧化钠溶液的产物不同
D. 将纯水加热,其KW增大而pH不变
【答案】A
【解析】
试题A、c( H+)>c(OH-)的溶液一定显酸性,符合溶液酸碱性的判断,正确;B、常温下,pH=6的溶液为酸性溶液,但不一定是酸溶液,可能是强酸弱碱盐溶液,错误;C、电解稀硫酸或氢氧化钠溶液的实质都是电解水,产物都是氢气和氧气,错误;D、将纯水加热,水的电离平衡正向移动,氢离子和氢氧根离子浓度都增大,水的离子积增大,但pH减小,错误,答案选A。

【题目】钠硫电池作为一种新型储能电池,其应用逐渐得到重视和发展。
(1)Al(NO3)3是制备钠硫电池部件的原料之一。由于Al(NO3)3容易吸收环境中的水分,需要对其进行定量分析。具体步骤如下图所示:
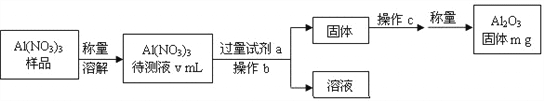
①加入过量试剂a,发生反应的离子方程式为___________________________。
②生成氧化铝的化学反应方程式是_______________________________________。
③Al(NO3)3待测液中,c (Al3+) = ______mol·L-1(用m、v表示)。
(2)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如下图所示:
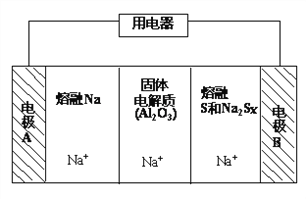
①据下表数据,请你判断该电池工作的适宜温度应控制在____范围内(填字母序号)。
a .100℃以下 b . 300℃~ 350℃ c. 100℃~ 300℃ d. 350℃~ 2050℃
物质 | Na | S | Al2O3 |
熔点/℃ | 97.8 | 115 | 2050 |
沸点/℃ | 892 | 444.6 | 2980 |
②该电池工作时,2Na + xS(3<x<5)=Na2Sx,则电极A上发生的电极反应式是_______。
内电路中Na+的移动方向为_________(填“从A到B”或“从B到A”)。