题目内容
【题目】在一定温度下,向5L密闭容器中加入2mol Fe(s)与1mol H2O(g),t1秒时,H2的物质的量为0.20mol,到第t2秒时恰好达到平衡,此时H2的物质的量为0.35mol.
(1)t1~t2这段时间内的化学反应速率v(H2)=________
(2)保持温度不变,若继续加入2mol Fe(s),则平衡移动________ (填“向正反应方向”、“向逆反应方向”或“不”),继续通入1mol H2O(g)再次达到平衡后,H2物质的量为________ mol.
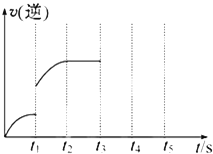
(3)该反应在t3时刻改变了某种条件使逆反应速率增大,改变的条件可能是________(任填一个即可)
(4)该反应的平衡常数表达式________
【答案】0.03/(t2-t1)molL﹣1s﹣1 不 0.7 升高温度 ![]()
【解析】
铁与水蒸气反应的方程式为3Fe(s)+4H2O(g)Fe3O4 (s)+4H2 (g),该反应前后气体分子数不发生变化,故在一定的范围内改变压强不会使平衡发生移动。该反应的平衡常数表达式为:K![]() 。
。
(1)t1 ~t2 这段时间内氢气的浓度变化为:0.35mol-0.20mol=0.15mol,这段时间内的化学反应速率v(H2)=0.15/[5×(t2- t1)]= 0.03/(t2-t1)molL﹣1s﹣1;综上所述,本题答案是:0.03/(t2-t1)molL﹣1s﹣1。
(2)在固体有剩余的情况下,增加或减少固体的质量,对反应速率以及限度均无影响;再加入1molH2O(g) 再次达到平衡时,平衡常数不变,故H2 的物质的量为原来的2倍,即:H2 物质的量为0.35×2=0.7mol;综上所述,本题答案是:不;0.7。
(3)t1 时反应未达到平衡,改变条件后逆反应速率突然增大,且继续增大,改变的条件为升高温度;综上所述,本题答案是:升高温度。
(4)铁与水蒸气反应的方程式为:3Fe(s)+4H2O(g)Fe3O4(s)+4H2(g),平衡常数表达式为:K![]() ;综上所述,本题答案是: K
;综上所述,本题答案是: K![]() 。
。