题目内容
【题目】某工厂拟综合处理含NH4+ 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
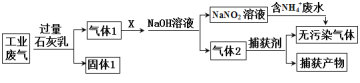
下列说法不正确的是
A.X可以是过量的空气
B.固体1中主要含有Ca(OH)2、CaCO3、CaSO3
C.捕获剂所捕获的气体主要是CO
D.处理含NH4+ 废水,每产生1mol无污染气体转移3NA电子
【答案】A
【解析】
工业废气中CO2、SO2可被石灰水吸收,生成固体1为CaCO3、CaSO3,气体1是不能被过量石灰水吸收的N2、NO、CO,气体1通入气体X,用氢氧化钠溶液处理后到的NaNO2,X可为空气,但不能过量,否则得到硝酸钠,NaNO2与含有NH4+的溶液反应生成无污染气体,应生成氮气,则气体2含有CO、N2,捕获剂所捕获的气体主要是CO。
A. 由分析可知,气体1是不能被过量石灰水吸收的N2、NO、CO,气体1通入气体X,用氢氧化钠溶液处理后到的NaNO2,X可为空气,但不能过量,否则得到硝酸钠,故A错误;
B. 工业废气中CO2、SO2可被石灰水吸收,生成CaCO3、CaSO3,因氢氧化钙过量,则固体1为主要含有Ca(OH)2、CaCO3、CaSO3,故B正确;
C. 气体2含有CO、N2,经捕获剂得到N2和CO,所捕获的气体主要是CO,防止污染空气,故C正确;
D. NaNO2与含有NH4+的溶液反应生成无污染气体,应生成氮气,发生氧化还原反应,离子方程式为NH4+ +NO2 = N2↑+2H2O,故D正确。
综上所述,答案为A。

【题目】铬铁矿的主要成分可表示为FeOCr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:
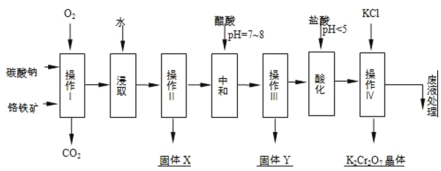
已知:
①4FeOCr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2↑;
8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3![]() 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
根据题意回答下列问题:
(1)操作I在常温下该反应速度极慢,下列措施中能使反应速率增大的是______.
A.升高温度 B.通入过量的空气 C.将原料粉碎 D.增加纯碱的用量
(2)固体X中主要含有______(填写化学式);
(3)酸化步骤用盐酸调节溶液pH<5,并煮沸其目的是______.(离子方程式表示)
(4)操作 iv有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、______、______、洗涤、干燥.
(5)表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl.
该反应在溶液中能发生的理由是______.(文字说明)
物质 | 溶解度/(g/100g水) | ||||
0°C | 40°C | 80°C | |||
KCl | 28 | 40.1 | 51.3 | ||
NaCl | 35.7 | 36.4 | 38 | ||
K2Cr2O7 | 4.7 | 26.3 | 73 | ||
Na2Cr2O7 | 163 | 215 | 376 | ||
(6)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量______(填写试剂)、溶解、过滤、再______(填写试剂)、…灼烧、冷却、称量,得干燥固体m g.计算样品中氢氧化铝的质量分数为______(用含m、n的代数式表示).