题目内容
【题目】某温度下,反应:H2(g) + CO2(g)![]() H2O(g)+CO(g)的平衡常数K =9/4该温度下,在甲、乙两个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
H2O(g)+CO(g)的平衡常数K =9/4该温度下,在甲、乙两个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
起始浓度 | 甲 | 乙 |
c(H2)/mol L-1 | 0.010 | 0.020 |
C(CO2)/mol·L-1 | 0.010 | 0.010 |
下列判断正确的是
A. 平衡时,甲容器中H2的转化率为60%
B. 平衡时,乙容器中H2的转化率大于60%
C. 平衡时,乙容器中c(H2)是甲容器中的2倍
D. 反应开始时,甲容器中的反应速率比乙容器中的反应速率快
【答案】A
【解析】试题分析:A、甲和丙对比,并相当于是在甲的基础上又加倍增大了物质的加入量,但是对于化学反应前后体积不变的反应,增大压强,化学平衡不移动,物质的转化率不变,设甲容器中平衡时二氧化碳的转化为xmol/L,根据K=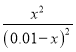 =
=![]() ,得x=0.006,所以CO2的转化率为60%,H2的转化率也是60%,所以丙中H2的转化率均是60%,故A正确;B、乙和甲对比,乙相当于在甲的基础上增加了氢气的量,所以乙中二氧化碳的转化率增大,会大于甲中的,即大于60%,故B错误;C、甲和丙对比,并相当于是在甲的基础上又加倍增大了物质的加入量,但是对于化学反应前后体积不变的反应,增大压强,化学平衡不移动,丙的初始投入量是甲的2倍,所以平衡时,丙中c(CO2)是甲中的2倍,设甲容器中平衡时二氧化碳转化为xmol/L,根据K=
,得x=0.006,所以CO2的转化率为60%,H2的转化率也是60%,所以丙中H2的转化率均是60%,故A正确;B、乙和甲对比,乙相当于在甲的基础上增加了氢气的量,所以乙中二氧化碳的转化率增大,会大于甲中的,即大于60%,故B错误;C、甲和丙对比,并相当于是在甲的基础上又加倍增大了物质的加入量,但是对于化学反应前后体积不变的反应,增大压强,化学平衡不移动,丙的初始投入量是甲的2倍,所以平衡时,丙中c(CO2)是甲中的2倍,设甲容器中平衡时二氧化碳转化为xmol/L,根据K=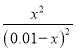 =
=![]() ,得x=0.006,则平衡时甲容器中c(CO2)是0.004mol/L,而甲和丙为等效平衡,但丙的起始浓度为甲的两倍,所以平衡时,丙中c(CO2)是0.008mol/L,故C错误;D、反应开始时,丙中的物质的浓度最大,反应速率最快,甲中的物质的浓度最小,反应速率最慢,故D错误;故选A。
,得x=0.006,则平衡时甲容器中c(CO2)是0.004mol/L,而甲和丙为等效平衡,但丙的起始浓度为甲的两倍,所以平衡时,丙中c(CO2)是0.008mol/L,故C错误;D、反应开始时,丙中的物质的浓度最大,反应速率最快,甲中的物质的浓度最小,反应速率最慢,故D错误;故选A。