题目内容
(2009?湘潭一模)下图所示反应有直接进行的,也有在溶液中进行的,其中部分产物已略去.已知:A是常见金属单质、H为气体单质,D溶于水是一种常见的强酸,一个D分子含有18个电子,Y是一种淡黄色固体粉末.
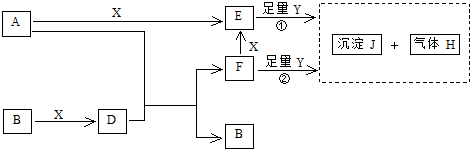
(1)写出化学式:B为
(2)写出D的电子式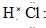
 ,液态D能否导电
,液态D能否导电
(3)A是一种非常重要的工业产品.据统计,地球上每年由于腐蚀而消耗的A约占A年产量的10%.A发生腐蚀的主要原因是(填写下面的选项序号)
a.直接与氧气发生化学腐蚀b.通过原电池反应发生腐蚀 c.因溶于水而消耗掉
若你选定选项a或c,请写出相应的化学方程式;若你选定选项b,请写出负极的电极反应式:
(4)①中所涉及的反应的化学方程式为:

(1)写出化学式:B为
H2
H2
,F为FeCl2
FeCl2
;(2)写出D的电子式
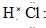
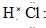
否
否
(填“能”或“否”);(3)A是一种非常重要的工业产品.据统计,地球上每年由于腐蚀而消耗的A约占A年产量的10%.A发生腐蚀的主要原因是(填写下面的选项序号)
b
b
;a.直接与氧气发生化学腐蚀b.通过原电池反应发生腐蚀 c.因溶于水而消耗掉
若你选定选项a或c,请写出相应的化学方程式;若你选定选项b,请写出负极的电极反应式:
Fe-2e-=Fe2+
Fe-2e-=Fe2+
;(4)①中所涉及的反应的化学方程式为:
2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑
,FeCl3+3NaOH=Fe(OH)3↓+3NaCl
FeCl3+3NaOH=Fe(OH)3↓+3NaCl
.分析:D溶于水是一种常见的强酸,一个D分子含有18个电子,可知D为HCl,由金属A与HCl反应生成B可知,B应为H2,则X为Cl2,F、E应为氯化物,且F可转化为E,可知A应为变价金属,为Fe,则E为FeCl3,F为FeCl2,Y是一种淡黄色固体粉末,应为Na2O2,由转化关系可知J为Fe(OH)3,H为O2,结合对应物质的性质以及题目要求解答该题.
解答:解:D溶于水是一种常见的强酸,一个D分子含有18个电子,可知D为HCl,由金属A与HCl反应生成B可知,B应为H2,则X为Cl2,F、E应为氯化物,且F可转化为E,可知A应为变价金属,为Fe,则E为FeCl3,F为FeCl2,Y是一种淡黄色固体粉末,应为Na2O2,由转化关系可知J为Fe(OH)3,H为O2,
(1)由以上分析可知B为H2,F为FeCl2,故答案为:H2; FeCl2;
(2)由以上分析可知D为HCl,为共价化合物,电子式为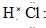 ,液态时不能电离出自由移动的离子,不能导电,故答案为:
,液态时不能电离出自由移动的离子,不能导电,故答案为: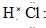 ;否;
;否;
(3)A为铁,易发生腐蚀而损耗,主要发生电化学腐蚀,发生原电池反应时,铁为负极,被氧化,电极方程式为Fe-2e-=Fe2+,故答案为:b; Fe-2e-=Fe2+;
(4)在氯化铁溶液中加入过氧化钠,过氧化钠与水反应生成氢氧化钠和氧气,氢氧化钠和氯化铁反应生成氢氧化铁,反应的方程式分别为2Na2O2+2H2O=4NaOH+O2↑,FeCl3+3NaOH=Fe(OH)3↓+3NaCl,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;FeCl3+3NaOH=Fe(OH)3↓+3NaCl.
(1)由以上分析可知B为H2,F为FeCl2,故答案为:H2; FeCl2;
(2)由以上分析可知D为HCl,为共价化合物,电子式为
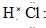 ,液态时不能电离出自由移动的离子,不能导电,故答案为:
,液态时不能电离出自由移动的离子,不能导电,故答案为: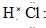 ;否;
;否;(3)A为铁,易发生腐蚀而损耗,主要发生电化学腐蚀,发生原电池反应时,铁为负极,被氧化,电极方程式为Fe-2e-=Fe2+,故答案为:b; Fe-2e-=Fe2+;
(4)在氯化铁溶液中加入过氧化钠,过氧化钠与水反应生成氢氧化钠和氧气,氢氧化钠和氯化铁反应生成氢氧化铁,反应的方程式分别为2Na2O2+2H2O=4NaOH+O2↑,FeCl3+3NaOH=Fe(OH)3↓+3NaCl,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;FeCl3+3NaOH=Fe(OH)3↓+3NaCl.
点评:本题考查无机物的推断,为高考常见题型,侧重于学生的分析能力的考查,注意把握题给信息以及相关元素化合物知识,把握题眼和推断的突破口,答题时注意体会并把握相关规律和方法,难度中等.

练习册系列答案
相关题目
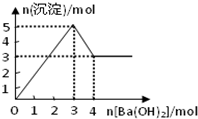 (2009?湘潭一模)如图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
(2009?湘潭一模)如图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
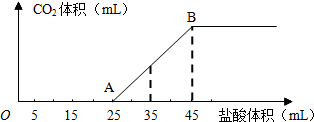 (2009?湘潭一模)将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol?L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
(2009?湘潭一模)将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol?L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示: