题目内容
有Na2CO3、NaHCO3、CaO和NaOH组成的混合物28.2g,把它们溶于足量的水,充分反应后,溶液中Ca2+、CO32-、HCO3-均转化为沉淀,将容器中的水分蒸干,最后得到白色固体物质共30g.则下列有关叙述错误的是( )
| A、原混合物中含Na2CO3 0.1mol |
| B、原混合物中n(Na2CO3)+n(NaHCO3)=n(CaO) |
| C、30g固体中一定存在n(CaCO3)>n(NaOH) |
| D、不能确定原混合物中NaOH的质量 |
考点:有关混合物反应的计算
专题:计算题
分析:充分反应后,溶液中Ca2+、CO32-、HCO3-均转化为沉淀,即为CaCO3,溶液中溶质为NaOH,将溶液蒸干,所得固体为CaCO3、NaOH混合物,发生反应为:
①CaO+H2O=Ca(OH)2
②Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
③NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O
将①+②得:CaO+H2O+Na2CO3=CaCO3↓+2NaOH ④
将①+③得:CaO+NaHCO3=CaCO3↓+NaOH ⑤
可以看做发生反应④、⑤,反应④即CaO 与Na2CO3 反应,由于H2O 参加反应,会引起固体质量增加,反应⑤即CaO 与NaHCO3 反应,不会引起固体质量增加,即:固体增加的质量等于参加反应的水的质量,
A.根据反应④计算碳酸钠的物质的量;
B.溶液中Ca2+、CO32-、HCO3-均转化为CaCO3,根据反应④⑤计算判断;
C.根据反应④⑤中生成的CaCO3、NaOH关系,结合原混合物中还含有NaOH,据此判断;
D.由于氢氧化钠在原混合物中存在,反应后又生成部分氢氧化钠,故不能确定氢氧化钠的量.
①CaO+H2O=Ca(OH)2
②Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
③NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O
将①+②得:CaO+H2O+Na2CO3=CaCO3↓+2NaOH ④
将①+③得:CaO+NaHCO3=CaCO3↓+NaOH ⑤
可以看做发生反应④、⑤,反应④即CaO 与Na2CO3 反应,由于H2O 参加反应,会引起固体质量增加,反应⑤即CaO 与NaHCO3 反应,不会引起固体质量增加,即:固体增加的质量等于参加反应的水的质量,
A.根据反应④计算碳酸钠的物质的量;
B.溶液中Ca2+、CO32-、HCO3-均转化为CaCO3,根据反应④⑤计算判断;
C.根据反应④⑤中生成的CaCO3、NaOH关系,结合原混合物中还含有NaOH,据此判断;
D.由于氢氧化钠在原混合物中存在,反应后又生成部分氢氧化钠,故不能确定氢氧化钠的量.
解答:
解:充分反应后,溶液中Ca2+、CO32-、HCO3-均转化为沉淀,即为CaCO3,溶液中溶质为NaOH,将溶液蒸干,所得固体为CaCO3、NaOH混合物,发生反应为:
①CaO+H2O=Ca(OH)2
②Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
③NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O
将①+②得:CaO+H2O+Na2CO3=CaCO3↓+2NaOH ④
将①+③得:CaO+NaHCO3=CaCO3↓+NaOH ⑤
可以看做发生反应④、⑤,反应④即CaO 与Na2CO3 反应,由于H2O 参加反应,会引起固体质量增加,反应⑤即CaO 与NaHCO3 反应,不会引起固体质量增加,即:固体增加的质量等于参加反应的水的质量,
A.参加反应水的质量=30g-28.2g=1.8g,其物质的量=
=0.1mol,由CaO+H2O+Na2CO3=CaCO3↓+2NaOH,可知碳酸钠的物质的量为0.1mol,故A正确;
B.根据反应④、⑤可知,CaO 与Na2CO3 按1:1反应,CaO 与NaHCO3也按1:1反应,故原混合物中n(Na2CO3)+n(NaHCO3)=n(CaO),故B正确;
C.反应④中CaCO3、NaOH为1:2、反应⑤中CaCO3、NaOH为1:1,且原混合物中还含有NaOH,故30g固体中一定存在n(CaCO3)<n(NaOH),故C错误;
D.由于氢氧化钠在原混合物中存在,反应后又生成部分氢氧化钠,故不能确定氢氧化钠的量,故D正确;
故选C.
①CaO+H2O=Ca(OH)2
②Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
③NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O
将①+②得:CaO+H2O+Na2CO3=CaCO3↓+2NaOH ④
将①+③得:CaO+NaHCO3=CaCO3↓+NaOH ⑤
可以看做发生反应④、⑤,反应④即CaO 与Na2CO3 反应,由于H2O 参加反应,会引起固体质量增加,反应⑤即CaO 与NaHCO3 反应,不会引起固体质量增加,即:固体增加的质量等于参加反应的水的质量,
A.参加反应水的质量=30g-28.2g=1.8g,其物质的量=
| 1.8g |
| 18g/mol |
B.根据反应④、⑤可知,CaO 与Na2CO3 按1:1反应,CaO 与NaHCO3也按1:1反应,故原混合物中n(Na2CO3)+n(NaHCO3)=n(CaO),故B正确;
C.反应④中CaCO3、NaOH为1:2、反应⑤中CaCO3、NaOH为1:1,且原混合物中还含有NaOH,故30g固体中一定存在n(CaCO3)<n(NaOH),故C错误;
D.由于氢氧化钠在原混合物中存在,反应后又生成部分氢氧化钠,故不能确定氢氧化钠的量,故D正确;
故选C.
点评:有关循环反应的计算中,采用整体思维分析法,可以使复杂问题简单化,我们采用整体思维分析就会发现,只要抓住起始、末了状态,列个总反应方程式,就会使得问题简单明了,难度较大.

练习册系列答案
相关题目
设NA为阿伏加德罗常数,下列叙述正确的是( )
| A、1mol?L-1 NaHCO3溶液中的Na+数为NA |
| B、常温时,2.24L CO2所含的氧原子数为0.2NA |
| C、5.6g Fe与足量稀盐酸反应,转移电子数为0.2NA |
| D、标准状况下,2.24L CCl4所含分子数为0.1NA |
下列表示对应化学反应的离子方程式或化学方程式正确的是( )
| A、向NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全:NH4++H++SO42-+Ba2++2OH-═NH3?H2O+BaSO4↓+H2O | ||||
| B、酸性高锰酸钾溶液与H2O2溶液混合:2MnO4-+3H2O2+6H+═2Mn2++6H2O+O2↑ | ||||
C、用铜作电极电解饱和食盐水:2Cl-+2H2O
| ||||
D、以下有机物在碱性条件下水解的化学方程式:BrCH2-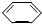 -OOCH+3NaOH -OOCH+3NaOH
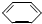 ONa+HCOONa+NaBr ONa+HCOONa+NaBr |
鉴别Clˉ、Brˉ、Iˉ三种离子,宜选用的试剂组是( )
| A、溴水和淀粉溶液 |
| B、硝酸银溶液和稀硝酸 |
| C、氯水和四氯化碳 |
| D、氯水和碘化钾淀粉溶液 |
PbO2在酸性溶液中能将Mn2+氧化成MnO4-,本身被还原为Pb2+.取一支试管,加入适量PbO2固体和适量的稀H2SO4后滴入2mL 1mol/L MnSO4溶液.下列说法错误的是( )
| A、充分振荡后静置,溶液颜色变为紫色 |
| B、上述实验中不能用盐酸代替硫酸 |
| C、在酸性条件下,PbO2的氧化性比MnO4-的氧化性强 |
| D、若上述实验完全反应,消耗PbO2的物质的量为0.01mol |
2014年5月21日,中俄签订了30年天然气供应合同,成为我国得到清洁能源的主要来源.天然气的主要成分是( )
| A、CH4 |
| B、C2H4 |
| C、CO |
| D、H2 |