题目内容
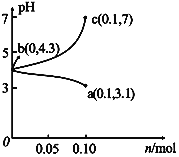
【题目】25℃时, H3A 水溶液(一种酸溶液)中含 A 的各种粒子的分布分数(平衡时某种粒子的浓度占各种粒子浓度之和的分数(α)与 pH 的关系如图所示。下列叙述正确的是( )
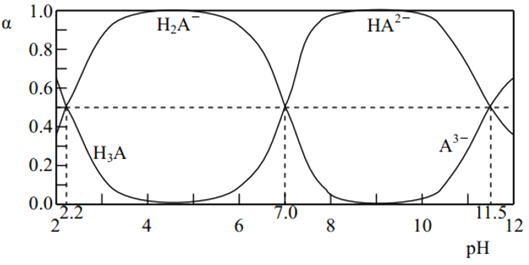
A. 根据图,可得 Ka1(H3A )≈10-7
B. 将等物质的量的 NaH2A 和 Na2HA 混合物溶于水,所得的溶液中 α(H2Aˉ)=α(HA2-)
C. 以酚酞为指示剂(变色范围 pH 8.2~10.0),将 NaOH 溶液逐滴加入到 H3A 溶液中,当溶液由无色变为浅红色时停止滴加,则生成 NaH2A
D. 在上述含 A 的各种粒子的体系中,若 c(H2Aˉ)+5c(A3ˉ)+c(OHˉ)=c(H+),则溶液pH为11.5
【答案】B
【解析】从图像可知H3A 为弱酸,存在电离平衡,H3A![]() H2A-+H+, 当溶液的pH=2.2时,c(H3A)= c(H2A-), c(H+)=10-2.2,带入数据计算电离平衡常数Ka1(H3A )= c(H2A-)×c(H+)/ c(H3A)=10-2.2,A错误;将等物质的量的 NaH2A 和 Na2HA 混合物溶于水,溶液呈中性,说明NaH2A电离显酸性,Na2HA水解显碱性,由于c(OHˉ)=c(H+),说明H2A-电离能力与HA-水解能力相等,所得的溶液中 α(H2Aˉ)=α(HA2-),B正确;根据图像可知,以酚酞为指示剂(变色范围 pH 8.2~10.0),碱性环境下生成Na2HA溶液,C错误;如果溶液的pH为11.5,该溶液为碱性溶液,应该满足c(OHˉ)> c(H+),不会出现c(H2Aˉ)+5c(A3ˉ)+c(OHˉ)=c(H+)这样关系式,D错误;正确选项B。
H2A-+H+, 当溶液的pH=2.2时,c(H3A)= c(H2A-), c(H+)=10-2.2,带入数据计算电离平衡常数Ka1(H3A )= c(H2A-)×c(H+)/ c(H3A)=10-2.2,A错误;将等物质的量的 NaH2A 和 Na2HA 混合物溶于水,溶液呈中性,说明NaH2A电离显酸性,Na2HA水解显碱性,由于c(OHˉ)=c(H+),说明H2A-电离能力与HA-水解能力相等,所得的溶液中 α(H2Aˉ)=α(HA2-),B正确;根据图像可知,以酚酞为指示剂(变色范围 pH 8.2~10.0),碱性环境下生成Na2HA溶液,C错误;如果溶液的pH为11.5,该溶液为碱性溶液,应该满足c(OHˉ)> c(H+),不会出现c(H2Aˉ)+5c(A3ˉ)+c(OHˉ)=c(H+)这样关系式,D错误;正确选项B。

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目