题目内容
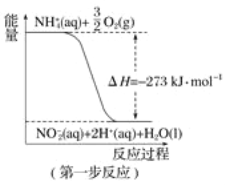
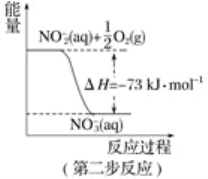
【题目】设NA表示阿伏加德罗常数的值。下列叙述正确的是
A. 4.0g由CO2和SO2组成的混合物中含有的质子数为2NA
B. 2.24LCl2与CH4在光照下反应生成的HCl分子数为0.1NA
C. 常温下,0.1mol环氧乙烷(![]() )中含有的共价键数为0.3NA
)中含有的共价键数为0.3NA
D. 4.2gCaH2与水完全反应,转移的电子数为0.1NA
【答案】A
【解析】
A.4.0g CO2中含有的质子数为![]() ,4.0gSO2中含有的质子数为
,4.0gSO2中含有的质子数为![]() ,因此4.0g由CO2和SO2 组成的混合物中含有的质子数也为2NA,故A正确;
,因此4.0g由CO2和SO2 组成的混合物中含有的质子数也为2NA,故A正确;
B.未说标准状况,无法计算,故B错误;
C.不要忽略C-H键,0.1mol环氧乙烷(![]() )中含有的共价键数应该为7NA,故C错误;
)中含有的共价键数应该为7NA,故C错误;
D. 4.2gCaH2与水完全反应,化学方程式为CaH2+2H2O=Ca(OH)2+2H2↑转移的电子的物质的量为![]() 0.2mol,故D错误;
0.2mol,故D错误;
答案:A

 小学教材全测系列答案
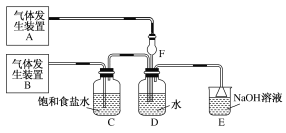
小学教材全测系列答案【题目】CCl3CHO是一种药物合成的中间体,可通过CH3CH2OH+4Cl2→CCl3CHO+5HCl进行制备。制备时可能发生的副反应为C2H5OH+HCl→C2H5Cl+H2O、CCl3CHO+HClO→CCl3COOH+HCl。合成该有机物的实验装置示意图(加热装置未画出)和有关数据如下:
物质 | C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl |
熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇 | 微溶于水,可溶于乙醇 |
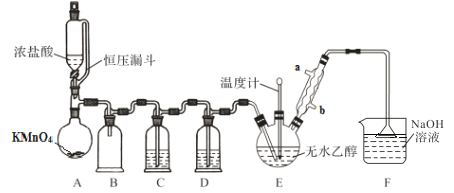
(1)恒压漏斗A的作用是________;A装置中发生反应的化学方程式为________。
(2)装置B的作用是________;装置F在吸收气体时,为什么可以防止液体发生倒吸现象。________。
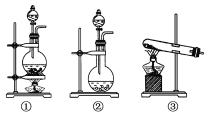
(3)装置E中的温度计要控制在70 ℃,三口烧瓶采用的最佳加热方式是______。如果要在球形冷凝管中注入冷水增加冷凝效果,冷水应该从________(填“a”或“b”)口通入。实验使用球形冷凝管而不使用直形冷凝管的目的是_______。
(4)实验中装置C中的试剂是饱和食盐水,装置中D的试剂是浓H2SO4。如果不使用D装置,产品中会存在较多的杂质________(填化学式)。除去这些杂质最合适实验方法是_______。
(5)利用碘量法可测定产品的纯度,反应原理如下:
CCl3CHO+NaOH=CHCl3+HCOONa HCOONa+I2=HI+NaI+CO2↑ I2+2Na2S2O3=2NaI+Na2S4O6
称取该实验制备的产品5.00 g,配成100.00 mL溶液,取其中10.00 mL,调节溶液为合适的pH后,加入30.00 mL 0.100 mol·L1的碘标准液,用0.100 mol·L1的Na2S2O3溶液滴定,重复上述3次操作,消耗Na2S2O3溶液平均体积为20.00 mL,则该次实验所得产品纯度为________。