题目内容
【题目】CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是( )
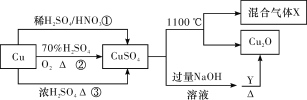
A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3∶2
B.相对于途径①、③,途径②更好地体现了绿色化学思想
C.1 mol CuSO4在1100 ℃所得混合气体X中O2为0.75 mol
D.Y可以是葡萄糖
【答案】C
【解析】
试题分析:A、途径①的反应的离子方程式为3Cu+8H++2NO3-=3Cu2++3NO↑+4H2O,因此硫酸和硝酸的物质的量比值为3:2,故说法正确;B、途径②发生的反应是2Cu+O2+2H2SO4=2CuSO4+2H2O,途径③Cu+2HSO4(浓)=CuSO4+SO2↑+2H2O,途径①、③均有对环境有污染的气体产生,途径②没有,故说法正确;C、4CuSO4![]() 2Cu2O+O2↑+4SO3↑,消耗1molCuSO4生成0.25mol氧气,故说法错误;D、这是醛基被新制氢氧化铜悬浊液氧化的过程,葡萄糖中含有醛基,故说法正确。
2Cu2O+O2↑+4SO3↑,消耗1molCuSO4生成0.25mol氧气,故说法错误;D、这是醛基被新制氢氧化铜悬浊液氧化的过程,葡萄糖中含有醛基,故说法正确。

 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案【题目】根据要求完成下列实验过程(a、b为弹簧夹,加热及固定装置已略去)。
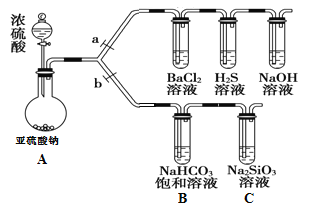
(1)验证SO2的氧化性、还原性和酸性氧化物的通性。
①连接仪器、_______________、加药品后,打开a、关闭b,然后滴入浓硫酸。
②装置A中发生的化学方程式是____________ ___。
③验证SO2的氧化性的实验现象是_____________ __。
④BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
滴加的溶液 | 氨水 | 氯水 |
沉淀的化学式 |
(2)验证碳、硅非金属性的相对强弱。
①在(1)①操作后打开b,关闭a。
②NaHCO3饱和溶液中发生的离子反应方程式为____________ ___。
③实验过程中,C中出现白色沉淀。甲同学认为不能由此说明碳的非金属性比硅强,需增加一个实验装置才能获得可靠实验结论,其改进方法为__________ 。


