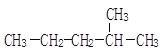题目内容
【题目】环戊二烯(![]() )可用于制备二茂铁(
)可用于制备二茂铁(![]() ,结构简式为
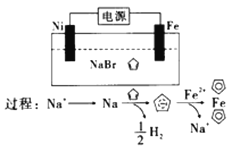
,结构简式为![]() ),后者广泛用于航天、化工等领域。二茂铁的电化学制备原理如图所示,下列说法正确的是( )
),后者广泛用于航天、化工等领域。二茂铁的电化学制备原理如图所示,下列说法正确的是( )
A. ![]() 为电解池的阳极
为电解池的阳极
B. 电解质溶液可以是![]() 的水溶液
的水溶液
C. 电解池的总反应方程式为:![]()
D. 电解质溶液中,当有![]() 的
的![]() 向
向![]() 电极移动时,同时在
电极移动时,同时在![]() 电极上产生了
电极上产生了![]() 的氢气
的氢气
【答案】C
【解析】
根据转化关系可知,需要获得Fe2+,则阳极为Fe电极,阴极为Ni,阴极上钠离子先得到电子生成金属Na,然后钠与环戊二烯反应生成氢气,实质为氢离子得到电子,阳极上Fe失去电子生成亚铁离子,中间产物Na与水反应,且水解水时生成的氢氧根离子与亚铁离子反应,影响了反应产物。
A、依据反应过程,可发现铁做阳极,![]() ,
,![]() 做阴极,故A错误;
做阴极,故A错误;
B、在整个过程中,![]() 做催化剂,由于有钠单质生成,因此,必须是无水的环境,故B错误;
做催化剂,由于有钠单质生成,因此,必须是无水的环境,故B错误;
C、![]() 得到电子转化为钠单质,钠单质再与环戊二烯发生反应,环戊二烯失去电子和
得到电子转化为钠单质,钠单质再与环戊二烯发生反应,环戊二烯失去电子和![]() 结合生成二茂铁,故C正确;
结合生成二茂铁,故C正确;
D、没有标明气体的状态,故D错误;
故选C。

【题目】某工厂的氨氮废水中主要含有![]() ,可用电化学氧化法加以处理。
,可用电化学氧化法加以处理。
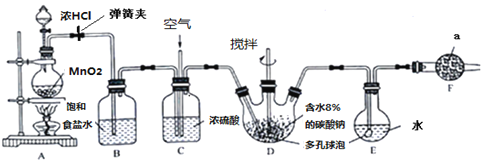
(1)图1是电化学氧化法的原理示意图。a的电极反应式是_____________。
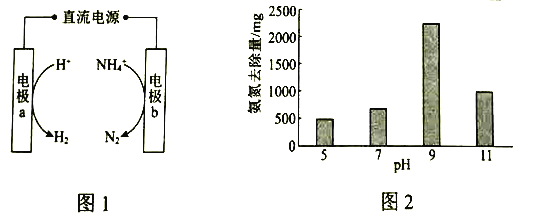
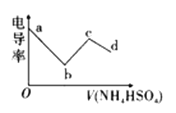
(2)研究显示,其他条件不变时,不同![]() 下氨氮的去除量如图2所示。已知:
下氨氮的去除量如图2所示。已知:![]() 与
与![]() 相比,在电极表面的吸附效果更好。结合平衡移动原理和图中数据,解释
相比,在电极表面的吸附效果更好。结合平衡移动原理和图中数据,解释![]() 从5到9时氨氮去除量增大的原因:______________。
从5到9时氨氮去除量增大的原因:______________。
(3)在电解废水的过程中,![]() 会经历“
会经历“![]() ”的过程。其他条件相同、
”的过程。其他条件相同、![]() 的浓度不同时,废水中氨氮脱除效率的实验结果如下:
的浓度不同时,废水中氨氮脱除效率的实验结果如下:
| 400 | 100 |
电解时间/h | 0.5 | 0.5 |
氨氮脱除效率/( | 2.40.8 |
①其它条件相同、适当提高![]() 的浓度,可以显著增大废水中
的浓度,可以显著增大废水中![]() 的脱除效率。
的脱除效率。
用化学用语解释原因:____________、![]() 。
。
②图2中,![]() 时,废水中
时,废水中![]() 去除量下降,可能的原因是:_______________。
去除量下降,可能的原因是:_______________。