题目内容
17.化学反应中的能量变化是由化学反应中旧化 学键断裂时吸收的能量与新化学键形成时放出 的能量不同引起的.如图为 N2(g)和 O2(g)反应生 成 NO(g)过程中的能量变化:
下列说法正确的是( )
| A. | 1 mol N2(g)和 1 mol O2(g)反应放出的能量为 180 kJ | |
| B. | 1 mol N2(g)和 1 mol O2(g)具有的总能量小于 2 mol NO(g)具有的总能量 | |
| C. | 通常情况下,N2(g)和 O2(g)混合能直接生成 NO(g) | |
| D. | NO 是一种酸性氧化物,能与 NaOH 溶液反应生成盐和水 |
分析 A、分析能量变化黑球代表氧原子,依据反应焓变=反应物断裂化学键吸收的能量-生成物形成化学键放出的能量计算判断;
B、依据A计算的焓变判断反应能量变化,结合反应前后能量守恒分析;
C、氮气和氧气在放电条件才能反应;
D、一氧化氮不能和氢氧化钠反应.
解答 解:A、焓变=反应物断裂化学键吸收的能量-生成物形成化学键放出的能量,N2+O2=2NO,△H=946KJ/mol+498KJ/mol-2×632KJ/mol=180KJ/mol,反应是吸热反应,故A错误;
B、依据A计算可知反应是吸热反应,依据能量守恒,1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量,故B正确;
C、通常情况下,N2(g)和O2(g)混合不能直接生成NO,故C错误;
D、一氧化氮不能和氢氧化钠反应,不是酸性氧化物,故D错误;
故选B.
点评 本题考查了反应能量变化的计算和判断,反应的焓变计算方法和能量守恒是解题关键,题目难度中等.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
2.海洋中有丰富的食品、矿产、药物和水产等资源,下列有关说法正确的是( )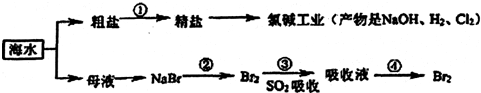

| A. | 海水淡化的主要方法有蒸馏法、电渗析法、离子交换法等 | |
| B. | 第①步中除去粗盐中可溶性杂质,可依次加入Na2CO3、Ba(OH)2、盐酸等试剂 | |
| C. | 在第②③④步中溴元素均被氧化 | |
| D. | 第④步涉及的分离操作有过滤、萃取、蒸馏 |
9.C6H12O2属于酯类的同分异构体共有( )种.
| A. | 20 | B. | 21 | C. | 22 | D. | 24 |
6.两种微粒含有相同的质子数和电子数,这两种微粒不可能是( )
①两种不同的原子
②两种元素的原子
③一种原子和一种分子
④一种原子和一种离子
⑤两种不同的分子
⑥一种分子和一种离子
⑦一种阴离子和一种阳离子.
①两种不同的原子
②两种元素的原子
③一种原子和一种分子
④一种原子和一种离子
⑤两种不同的分子
⑥一种分子和一种离子
⑦一种阴离子和一种阳离子.
| A. | ①③⑤⑦ | B. | ②④⑥⑦ | C. | ①③④⑤⑦ | D. | 全部都是 |
7.下列金属制品中最不容易被酸雨腐蚀的是( )
| A. | 镀锌水管 | B. | 铜制器皿 | C. | 铁制栏杆 | D. | 铝合金门窗 |
 如图装置,用电化学原理制备硫酸,并电解500mL 0.2mol?L-1AgNO3溶液.请回答下列问题:
如图装置,用电化学原理制备硫酸,并电解500mL 0.2mol?L-1AgNO3溶液.请回答下列问题: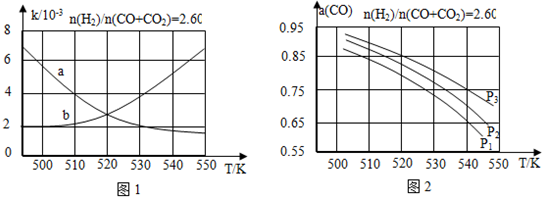
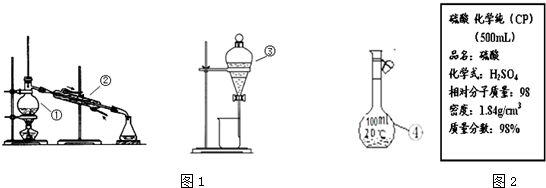
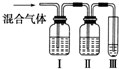 为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯,将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应.
为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯,将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应.