��Ŀ����
����Ŀ��ʵ���һ������÷Ͼ�����ӵ���������������(LiMn2O4)��һ����������:
(1)�Ͼɵ�ؿ��ܲ����е���ﮣ���ⲻ���ױ�ը���Ż�Ϊ�˰�ȫ���Բ�����Ҫ����____________��
(2)�������ʱ����HNO3��H2O2�Ļ��Һ�壬�ɽ����ܵ�LiMn2O4ת��ΪMn(NO3)2��LiNO3�Ȳ����д���÷�Ӧ���ӷ���ʽ___________________��
������������ܽ⣬�ӷ�Ӧ����ĽǶȷ��������������HNO3��H2O2������ȱ����____________��
(3)������2��ʱ��ϴ��Li2CO3�����IJ�����_______________________��
(4)�ѷ�����̼���������������ַ�ĩ�������ʵ���1:4��Ͼ��ȼ��ȿ���������LMn2O4�����µ�515��ʱ����ʼ��CO2������ͬʱ���ɹ���A����Ԥ��̼��﮵ķֽ��¶�(723��)�ͺܶ࣬���ܵ�ԭ����__________��
(5)�Ʊ��ߴ�MnCO3����:��֪MnCO3������ˮ���Ҵ�����ʪʱ�ױ�����������100�濪ʼ�ֽ⣻Mn(OH)2��ʼ������pH=7.7���벹�������������У��Ƶõ�Mn(OH)2�Ʊ��ߴ�MnCO3�IJ�������[ʵ���п�ѡ�õ��Լ�:H2SO4��Na2CO3��C2H5OH]����Mn(OH)2�б߽������_________________��
���𰸡� ����������ˮ�� 2LiMn2O4 +10 H+ +3H2O2 ��4Mn2++2 Li+ +3O2��+ 8H2O ��Ӧ���� Cl2����Ⱦ���� ���Ų�������������м�������ˮ����û��������ˮ��Ȼ�������ظ����� 2~3 �� ����������Ϊ������������̼��﮷ֽ��¶� H2SO4��Һ�������ܽ⣬���� Na2CO3����������Һ pH��7.7�����ˣ����������Ҵ�ϴ�ӣ����� 100����ո���
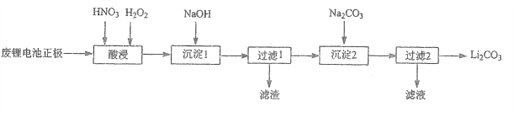
�������������������ԷϾ������������������﮵���������Ϊ���壬�������̵ķ��������ӷ���ʽ����д������ʵ������������Ʊ�ʵ�鷽������ơ��������ʱ����HNO3��H2O2�Ļ��Һ�壬�ɽ����ܵ�LiMn2O4ת��ΪMn��NO3��2��LiNO3�Ȳ��������1������NaOH��Mn��NO3��2ת���ɳ�����������2������Na2CO3��Li+�γ�Li2CO3������
��1��Li������е�O2��ˮ��Ӧ��
��2��HNO3��H2O2�Ļ��Һ��LiMn2O4��ԭΪMn��NO3��2����H2O2��������O2�����������HNO3��H2O2�Ļ��Һ���������������ΪCl2��
��3��ϴ�ӵIJ��������Ų�������������м�������ˮ����û��������ˮ��Ȼ�������ظ����� 2~3 ����
��4��MnO2��Ϊ������������̼��﮵ķֽ��¶ȡ�
��5��������Ŀ�ṩ���Լ��������Ʊ�MnCO3��ԭ��Ϊ��Mn��OH��2+H2SO4=MnSO4+2H2O��MnSO4+Na2CO3=MnCO3��+Na2SO4��pH=7.7ʱ��ʼ�γ�Mn��OH��2����������Na2CO3����Mn2+ʱ����pH![]() 7.7������MnCO3���������ʺͻ�ѧ����ѡ��MnCO3�����ᴿ�ķ�����
7.7������MnCO3���������ʺͻ�ѧ����ѡ��MnCO3�����ᴿ�ķ�����
�������1���Ͼɵ�ؿ��ܲ����е���ﮣ�﮻�ѧ���ʻ��ã�﮿�������е�O2��H2O��Ӧ���Բ���Ҫ����������������ˮ�֡�
��2���������ʱ����HNO3��H2O2�Ļ��Һ�壬�ɽ����ܵ�LiMn2O4ת��ΪMn��NO3��2��LiNO3�Ȳ�����LiMn2O4����ԭ��Mn��NO3��2����H2O2��������O2����Ӧ��1molLiMn2O4���뷴Ӧ�õ�3mol������1molH2O2ʧȥ2mol���ӣ����ݵ�ʧ�����غ��ԭ���غ㣬��Ӧ�Ļ�ѧ����ʽΪ2LiMn2O4+10HNO3+3H2O2=2LiNO3+4Mn��NO3��2+3O2��+8H2O����Ӧ�����ӷ���ʽΪ2LiMn2O4+10H++3H2O2=2Li++4Mn2++3O2��+8H2O�������������ܽ⣬��������ԭ����������Cl2�����������HNO3��H2O2������ȱ���ǣ���Ӧ����Cl2����Ⱦ������
��3��������2��ʱ��ϴ��Li2CO3�����IJ����ǣ����Ų�������������м�������ˮ����û��������ˮ��Ȼ�������ظ����� 2~3 ����
��4����������̼�����MnO2�����ʵ���1:4��Ͼ������µ�515��ʱ����ʼ��CO2��������Ԥ�Ƶ�̼��﮵ķֽ��¶ȵͺܶ࣬���ܵ�ԭ���ǣ�MnO2��Ϊ������������̼��﮵ķֽ��¶ȡ�
��5��������Ŀ�ṩ���Լ��������Ʊ�MnCO3��ԭ��Ϊ��Mn��OH��2+H2SO4=MnSO4+2H2O��MnSO4+Na2CO3=MnCO3��+Na2SO4��pH=7.7ʱ��ʼ�γ�Mn��OH��2����������Na2CO3����Mn2+ʱ����pH![]() 7.7���Ʊ�MnCO3�IJ���Ϊ����Mn��OH��2�м���H2SO4�������ܽ�ת��ΪMnSO4��Һ����MnSO4��Һ�м���Na2CO3����pH
7.7���Ʊ�MnCO3�IJ���Ϊ����Mn��OH��2�м���H2SO4�������ܽ�ת��ΪMnSO4��Һ����MnSO4��Һ�м���Na2CO3����pH![]() 7.7���MnCO3������������MnCO3������ˮ���Ҵ�����ʪʱ�ױ�����������100
7.7���MnCO3������������MnCO3������ˮ���Ҵ�����ʪʱ�ױ�����������100

 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д�

