题目内容
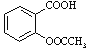
【题目】硼酸三甲酯用作柠檬类水果的熏蒸剂。实验室合成硼酸三甲酯的原理及装置如下:Na2B4O710H2O+2H2SO4+12CH3OH![]() 2NaHSO4+4(CH3O)3B+17H2O
2NaHSO4+4(CH3O)3B+17H2O
已知:
硼酸三甲酯 | 甲醇 | |
溶解性 | 与乙醚、甲醇混溶,能水解 | 与水混溶 |
沸点/℃ | 68 | 64 |
硼酸三甲酯与甲醇混合物的共沸点为54℃ | ||
实验步骤如下:
①在圆底烧瓶中加入44.8g甲醇和191.gNa2B4O710H2O(硼砂,式量为382),然后缓慢加入浓H2SO4并振荡;加热烧瓶中的液体;通过分馏柱回流一段时间。
②先接收51~55℃的馏分,再接收55~60℃的馏分。
③将两次馏分合并,加入氯化钙进行盐析分层,上层为硼酸三甲酯,分离。
④精馏得高纯硼酸三甲酯19.2g。
回答下列问题:
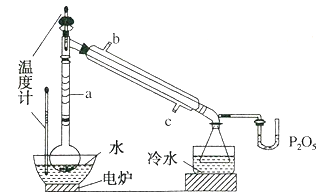
(1)图中仪器a的名称为__;直形冷凝管冷却水应从__(填“b”或“c”)接口进入。
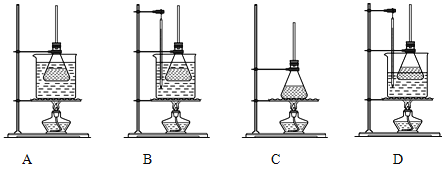
(2)本实验加热方式为__,优点是__。
(3)加入氯化钙盐析分层的主要目的是__。
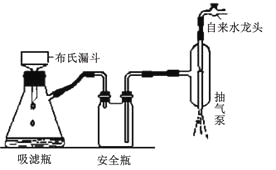
(4)U型管中P2O3的作用是__。
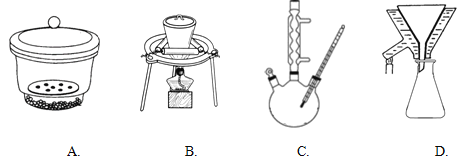
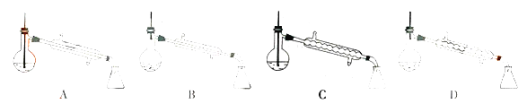
(5)图中,步骤④的仪器选择及安装都正确的是__,应收集__℃的馏分。
(6)本次实验的产率是__。
【答案】分馏柱 c 水浴加热 使物体受热均匀,便于控制温度 除去甲醇,避免精馏时形成恒沸物 防止空气中的水蒸气进入,导致硼酸三甲酯水解 b 68 92.3%
【解析】
(1)图中仪器a的名称为分馏柱,直形冷凝管冷却水应下进上出,所以应从c口进水,故答案为:分馏柱;c
(2)根据步骤![]() ,收集的是
,收集的是![]() 的馏分以及
的馏分以及![]() 的馏分,应采用水浴加热的方法,水浴加热的优点是可使受热物受热均匀,且更容易控制温度,故答案为:水浴加热;使物体受热均匀,便于控制温度
的馏分,应采用水浴加热的方法,水浴加热的优点是可使受热物受热均匀,且更容易控制温度,故答案为:水浴加热;使物体受热均匀,便于控制温度
(3)根据步骤![]() ,其目的是分离出硼酸三甲酯,而原先收集的是硼酸三甲酯和甲醇的混合物,因此加入氯化钙进行盐析分层的目的是除去甲醇,避免精馏时形成恒沸物,故答案为:除去甲醇,避免精馏时形成恒沸物;
,其目的是分离出硼酸三甲酯,而原先收集的是硼酸三甲酯和甲醇的混合物,因此加入氯化钙进行盐析分层的目的是除去甲醇,避免精馏时形成恒沸物,故答案为:除去甲醇,避免精馏时形成恒沸物;
(4)P2O5是一种常用的干燥剂,防止装置尾部一般是防止空气中的水蒸气进入,此处的目的应是避免硼酸三甲酯水解,故答案为:防止空气中的水蒸气进入,导致硼酸三甲酯水解
(5)步骤![]() 是精馏得到高纯硼酸三甲酯,ac装置温度计的位置不对,cd装置没有使用牛角管;硼酸三甲酯的沸点是
是精馏得到高纯硼酸三甲酯,ac装置温度计的位置不对,cd装置没有使用牛角管;硼酸三甲酯的沸点是![]() ,因此应收集
,因此应收集![]() 的馏分,故答案为:b;68
的馏分,故答案为:b;68
(6)圆底烧瓶中加入了![]() 甲醇和
甲醇和![]() ,根据所给的化学方程式计算可知,
,根据所给的化学方程式计算可知,![]() 完全反应需要甲醇
完全反应需要甲醇![]() ,因此,甲醇是过量的,根据
,因此,甲醇是过量的,根据![]() 计算,
计算,![]() 的物质的量为
的物质的量为![]() ,根据B原子守恒,理论上可制得硼酸三甲酯
,根据B原子守恒,理论上可制得硼酸三甲酯![]() ,质量为
,质量为![]() ,因此,其产率为
,因此,其产率为![]() ,故答案为:
,故答案为:![]() 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是:
A. 反应达到平衡时,X的转化率为50% B. 反应可表示为X+3Y![]() 2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数