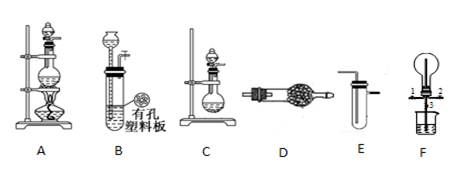
��Ŀ����
��15�֣�ԭ��������С�������е����ֶ�����Ԫ��X��Y��Z��W������Ԫ�ص�ԭ������֮��Ϊ32�������ڱ���X��ԭ�Ӱ뾶��С��Ԫ�أ�Y��Z�������ڣ�Z��Wλ��ͬ���塣
��1��XԪ�ط����� ��
��2��Z��W�γɵ���̬�⻯����ȶ���_______>_______��д��ѧʽ����
��3����X��Y��Z��W����Ԫ���е�������ɵ�һ��ǿ�ᣬ��ǿ���ϡ��Һ����ͭ��Ӧ�����ӷ���ʽΪ___________��
��4����X��Y��Z��W����Ԫ����ɵ�һ�����ӻ�����A����֪��1mol A��������NaOHŨ��Һ��Ӧ���ɱ�״����44.8L���塣��A�������ᷴӦ�������壬������������ˮ��Ӧ��д������������ˮ��Ӧ�����ӷ���ʽ_____________________��
��5����X��Y��Z��W��Fe����Ԫ����ɵ���Է�������Ϊ392�Ļ�����B��lmolB�к���6mol�ᾧˮ���Ի�����B��������ʵ�飺
A��ȡB����Һ�������ŨNaOH��Һ�����ȣ�������ɫ��������ɫ�̼�����ζ���壻��һ��ʱ���ɫ������Ϊ����ɫ�����ձ�Ϊ���ɫ��
B����ȡB����Һ���������BaCl2��Һ������ɫ������������������ܽ⡣
����ʵ��a��b��֪B��Һ�к��е�����Ϊ__________________��
��B�Ļ�ѧʽΪ_________________��
��15�֣�
��1��H��2�֣�
��2��H2O H2S��2�֣�
��3��3Cu+2NO3-+8H+=3Cu2++2NO��+4 H2O��3�֣�
��4��SO2+Cl2+ 2H2O= SO42-+2Cl-+4H+��3�֣�
��5����NH4+��Fe2+��SO42-��3�֣�
�ڣ�NH4��2Fe��SO4��2��6 H2O��2�֣�
���������������1�������ڱ���X��ԭ�Ӱ뾶��С��Ԫ�أ�����X��Ԫ�ط�����H��
��2����Z��ԭ��������x����Y��W��ԭ�������ֱ���x-1��x+8��������x+x+8+x-1+1=32�����x=8��Y��Z��W�ֱ���N��O��SԪ�ء�O�ķǽ�����ǿ��S������Z��W�γɵ���̬�⻯����ȶ���H2O>H2S��
��3����X��Y��Z��W����Ԫ���е�������ɵ�һ��ǿ�ᣬ��ǿ���ϡ��Һ����ͭ��Ӧ�����ǿ�������ᣬͭ��ϡ���ᷴӦ�����ӷ���ʽΪ3Cu+2NO3-+8H+=3Cu2++2NO��+4 H2O��
��4����H��N��O��S����Ԫ����ɵ�һ�����ӻ�����A�������������Ʒ�Ӧ�������壬˵��A�д���笠����ӣ�A���������ᷴӦ�������壬�Ҹ���������ˮ��Ӧ��˵���������ǻ�ԭ�����壬�ж�Ϊ�����������壬AΪ��NH4��2SO3���������������ˮ��Ӧ������������ᣬ���ӷ���ʽΪSO2+Cl2+ 2H2O= SO42-+2Cl-+4H+
��5����B��Ũ�Ӧ�����̼�����ζ�����壬˵��B�д���NH4+����Ӧ������ɫ������Ϊ����ɫ�����ձ�Ϊ���ɫ��˵��B�д���Fe2+���������BaCl2��Һ��������������İ�ɫ������˵��B�д���SO42-��
�ڸ���B���������ӵ����࣬�ж���3��������ɵĻ�ѧʽΪ��NH4��2Fe��SO4��2����lmolB�к���6mol�ᾧˮ������B�Ļ�ѧʽ�л���6 H2O������B�Ļ�ѧʽΪ��NH4��2Fe��SO4��2��6 H2O����B����Է���������392�����
���㣺����Ԫ���ƶϣ���ѧʽ�����ӷ���ʽ���жϼ���д��Ԫ������Ӧ�ã����ӵ��ж�

̼���仯�����й㷺����;��
��1���ڵ绯ѧ�У�����̼���缫��
��������п�̸ɵ���У�̼���� ����
������̼�����������缫��ⱥ��ʳ��ˮ�����ռ�ʱ��̼���� ������Ӧ�����ӷ���ʽ ��
��2����ˮ����ͨ�����ȵ�̼�ɲ���ˮú����C(s)+H2O(g)  CO(g)+H2(g) ��H=+131.3kJ/mol,�ﵽƽ����������ʱ�������H2O��ƽ��ת���ʵĴ�ʩ�� ��
CO(g)+H2(g) ��H=+131.3kJ/mol,�ﵽƽ����������ʱ�������H2O��ƽ��ת���ʵĴ�ʩ�� ��
| A�������¶� | B������̼������ |
| C��������� | D����CO���ռ���ȥCO |
 CO2(g)+H2(g)�õ��������ݣ�
CO2(g)+H2(g)�õ��������ݣ�| �¶�/�� | ��ʼŨ��mol/L | ƽ��Ũ��mol/L | |
| CO(g) | H2O(g) | H2(g) | |
| 900 | 2.0 | 0.8 | 0.4 |
ͨ�����㣬�÷�Ӧ��ƽ�ⳣ��Ϊ�� ��
��4����ҵ�ϰ�ˮú���еĻ�����崦����ýϴ���H2���ںϳɰ���
N2(g)+3H2(g)һ��������2NH3(g) ��H= ��92.4kJ/molijͬѧ�ڲ�ͬʵ��������ģ�⻯����������ʵ�飬N2Ũ����ʱ��仯��ͼ��
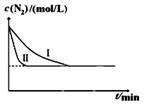
����ʵ��I�Ƚϣ�ʵ��II�ı������Ϊ�� ��
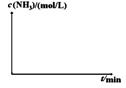
��ʵ��III��ʵ��I���¶�Ҫ�ߣ�����������ͬ��������ͼ����ʵ��I��ʵ��III��NH3Ũ����ʱ��仯��ʾ��ͼ��


 Si(s) + 2ZnCl2(l) ��H1 <0
Si(s) + 2ZnCl2(l) ��H1 <0 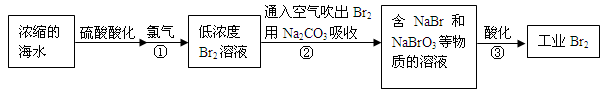

 ��������Ϊ����£�SO3������H2O����ʱ�ų�������Ϊ ��������λ��Ч���֣���
��������Ϊ����£�SO3������H2O����ʱ�ų�������Ϊ ��������λ��Ч���֣���