题目内容
4.下列实验与对应结论正确的是| A | B | C | D | |
装置 |  | 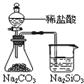 |  | 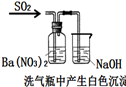 |
| 结论 | A.Ag2O/Ag极发生 还原反应 | B.能证明非金属性Cl>C>Si | C.验证铁发生析氢腐蚀 | D.白色沉淀是BaSO3 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
分析 A.正极上发生还原反应;
B.证明非金属性强弱的依据是最高价含氧酸的酸性强弱比较;
C.食盐水中发生吸氧腐蚀;
D.二氧化硫具有还原性,可与硝酸发生氧化还原反应.
解答 解:A.正极为Ag2O,原电池中电流从正极流向负极,负极上发生氧化反应,正极上发生还原反应,故A正确;
B.装置中盐酸和碳酸钠反应生成二氧化碳,只能说明盐酸酸性比碳酸强,但不能说明氯的非金属性强,二氧化碳通入硅酸钠能生成硅酸能说明碳酸酸性强于硅酸,碳酸和硅酸都是最高价含氧酸,能证明碳非金属性强于硅,故B错误;
C.氯化钠溶液呈中性,铁在食盐水中发生吸氧腐蚀,在酸性条件下发生析氢腐蚀,故C错误;
D.二氧化硫具有还原性,溶于水呈酸性,在酸性条件下可与硝酸根离子发生氧化还原反应,生成硫酸根离子,生成BaSO4,故D错误;
故选A.
点评 本题考查较为综合,涉及原电池、物质的性质以及分离提纯等知识,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意相关知识的学习与积累,难度不大.

练习册系列答案
相关题目
14.取50.0mLNa2CO3加入过量BaCl2溶液后,得到沉淀9.85g,将沉淀用过量稀HNO3处理后有气体放出.试计算:
(1)原溶液中Na2CO3的物质的量;
(2)产生气体的体积(标准状况下).
(1)原溶液中Na2CO3的物质的量;
(2)产生气体的体积(标准状况下).
15.下列对各物质的分类全部正确的是( )
| 酸性氧化物 | 碱性氧化物 | 酸 | 碱 | 强电解质 | 非电解质 | |
| A | NO2 | CuO | HF | KOH | H2SO4 | SO2 |
| B | CO2 | Na2O2 | HCl | Cu(OH)2 | HClO4 | CH4 |
| C | SiO2 | MgO | HClO | NH3•H2O | NaHCO3 | C2H5OH |
| D | Mn2O7 | K2O | HBr | Na2CO3 | Ba(OH)2 | Cl2 |
| A. | A | B. | B | C. | C | D. | D |
19.相关物质的溶度积常数见表:
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2•2H2O晶体,加入CuO、Cu(OH)2、CuCO3或 Cu2(OH)2CO3,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=2.6×10-9 mol•L-1.过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2•2H2O晶体.
(2)在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,原因是CuCl2•2H2O在加热时会发生水解(可能混有CuCl2、Cu(OH)2、Cu(OH)Cl、CuO等杂质),.由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是在干燥的HCl气流中加热脱水.
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀.用0.100 0mol•L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.已知:2Cu2++4I-=2CuI↓+I2; I2+2S2O32-=S4O62-+2I-.
①可选用淀粉溶液作滴定指示剂,滴定终点的现象是溶液蓝色褪去,且半分钟之内不恢复原色.
②该试样中CuCl2•2H2O的质量百分数为95%.
③若滴定终点时俯视滴定管刻度,则由此测得的CuCl2•2H2O的质量分数会偏小.(填“偏大”、“偏小”或“不变”,下同)
④若加入KI后,部分I-因被空气中的氧气氧化,则导致测得的CuCl2•2H2O的质量百分数的值会偏大.
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(2)在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,原因是CuCl2•2H2O在加热时会发生水解(可能混有CuCl2、Cu(OH)2、Cu(OH)Cl、CuO等杂质),.由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是在干燥的HCl气流中加热脱水.
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀.用0.100 0mol•L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.已知:2Cu2++4I-=2CuI↓+I2; I2+2S2O32-=S4O62-+2I-.
①可选用淀粉溶液作滴定指示剂,滴定终点的现象是溶液蓝色褪去,且半分钟之内不恢复原色.
②该试样中CuCl2•2H2O的质量百分数为95%.
③若滴定终点时俯视滴定管刻度,则由此测得的CuCl2•2H2O的质量分数会偏小.(填“偏大”、“偏小”或“不变”,下同)
④若加入KI后,部分I-因被空气中的氧气氧化,则导致测得的CuCl2•2H2O的质量百分数的值会偏大.
16.食品添加剂关系到人类健康.下列物质中的添加剂作用不正确的是( )
| A. | 食盐加碘:着色剂 | B. | 火腿中的NaNO3:防腐剂 | ||
| C. | 炒菜放味精:调味剂 | D. | 用小苏打发面蒸馒头:膨松剂 |
13.标准状况下,m g气体A和n g气体B的分子数相同,下列说法不正确的是( )
| A. | A与B的相对分子质量之比为m:n | |
| B. | 同质量的A与B分子个数之比为n:m | |
| C. | 同温同压下,两气体A与B的密度之比为n:m | |
| D. | 相同状况下,同体积的气体A与B质量比为m:n |
14.700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)═CO2(g)+H2(g).反应过程中测定的部分数据见表(表中t2>t1):
下列说法正确的是( )
| 反应时间/min | n(CO)/mol | H2O/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
| A. | 反应在t1min内的平均速率为v(H2)=$\frac{0.40}{{t}_{1}}$mol•L-1•min-1 | |
| B. | 保持其他条件不变,起始时向容器中充入0.60mol CO和1.20mol H2O,到达平衡时n(CO2)=0.30mol | |
| C. | 保持其他条件不变,向平衡体系中再通入0.20mol H2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大 | |
| D. | 温度升高至800℃,上述反应平衡常数为0.64,则正反应为吸热反应 |