题目内容
9.冶炼铁反应的平衡常数表达式K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$,温度升高后,K值减小(填“增大”、“不变”或“减小”).分析 Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=-28.5kJmol-1
依据平衡常数概念写出表达式,反应是吸热反应,升温平衡逆向进行.
解答 解:反应为Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=-28.5kJmol-1
平衡常数K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$;反应是放热反应,升温平衡逆向进行,平衡常数减小;
故答案为:$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$;减小;
点评 本题考查了热化学方程式和盖斯定律计算应用,平衡常数表达式,掌握基础是解题关键,题目较简单.

练习册系列答案
相关题目
19.微波是一种高频电磁振荡.微波炉就是利用高频电磁振荡使食品中粒子也产生振荡而发热,现代医学上使用的微波手术刀进行外科手术,其好处主要是使开刀处血液迅速凝固而减少失血,以下关于其作用原理的说法正确的是( )
| A. | 微波电流迅速中和血液胶体所带的电荷而凝固 | |
| B. | 微波使局部血液受热而使血液胶体凝固 | |
| C. | 微波电流通过手术刀时产生的高温使血液凝固 | |
| D. | 以上说法都正确 |
14.新型柴油发动机的受热面由耐高温且不易传热的材料制造.这种材料最可能是( )
| A. | 陶瓷 | B. | 不锈钢 | C. | 纯铁 | D. | 铝合金 |
1.热化学方程式S(l)+O2(g)═SO2(g);△H=-293.23kJ/mol.分析下列说法中不正确的是( )
| A. | S(s)+O2(g)═SO2(g),生成1mol SO2(g),反应放出的热量小于293.23 kJ | |
| B. | S(g)+O2(g)═SO2(g),生成1mol SO2(g),反应放出的热量大于293.23 kJ | |
| C. | 1 mol SO2的键能的总和大于1 mol 硫和1 mol 氧气的键能之和 | |
| D. | 1 mol SO2的键能的总和小于1 mol 硫和1 mol 氧气的键能之和 |
 工业制硫酸过程中,SO2催化氧化的原理为:2SO2(g)+O2(g)$?_{加热}^{催化剂}$2SO3(g)△H<0.按照相同的物质的量投料,测得SO2在不同温度下的平衡转
工业制硫酸过程中,SO2催化氧化的原理为:2SO2(g)+O2(g)$?_{加热}^{催化剂}$2SO3(g)△H<0.按照相同的物质的量投料,测得SO2在不同温度下的平衡转


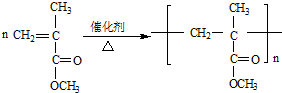 ;
;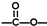 ”结构的链状化合物共有7种;
”结构的链状化合物共有7种;