题目内容
14.取50.0mLNa2CO3加入过量BaCl2溶液后,得到沉淀9.85g,将沉淀用过量稀HNO3处理后有气体放出.试计算:(1)原溶液中Na2CO3的物质的量;
(2)产生气体的体积(标准状况下).
分析 发生Na2CO3+BaCl2═BaCO3↓=2NaCl,BaCO3+2HNO3═Ba(NO3)2+H2O+CO2↑,沉淀9.85g为碳酸钡,结合反应及原子守恒计算.
解答 解:(1)由Na2CO3+BaCl2═BaCO3↓=2NaCl及沉淀9.85g为碳酸钡可知,n(Na2CO3)=n(BaCO3)=$\frac{9.85g}{197g/mol}$=0.05mol,
答:原溶液中Na2CO3的物质的量为0.05mol;
(2)发生反应BaCO3+2HNO3═Ba(NO3)2+H2O+CO2↑,由方程式可知n(CO2)=n(BaCO3)=0.05mol,故生成的二氧化碳的体积为0.05mol×22.4L/mol=1.12L,
答:产生的气体在标准状况下的体积为1.12L.
点评 本题考查化学反应方程式的计算,为高频考点,把握发生的反应及物质的量的有关计算为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
5.对于下列反应的反应类型的判断,不正确的是( )
| A. | CO2+H2O═H2CO3 化合反应 | |
| B. | Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O 分解反应 | |
| C. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2 置换反应 | |
| D. | NaCl+AgNO3═AgCl↓+NaNO3 复分解反应 |
9.盆栽鲜花一般需施用S-诱抗素制剂,以保证鲜花长期盛开.S-诱抗素的分子结构如图,下列关于该物质的说法正确的是( )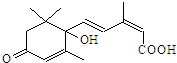

| A. | 该物质的分子式为C15H20O4 | |
| B. | 能发生消去反应 | |
| C. | 既能与FeCl3溶液发生显色反应,又能使溴水褪色 | |
| D. | 1mol该物质与NaOH溶液反应,最多可消耗1mol NaOH溶液 |
19.微波是一种高频电磁振荡.微波炉就是利用高频电磁振荡使食品中粒子也产生振荡而发热,现代医学上使用的微波手术刀进行外科手术,其好处主要是使开刀处血液迅速凝固而减少失血,以下关于其作用原理的说法正确的是( )
| A. | 微波电流迅速中和血液胶体所带的电荷而凝固 | |
| B. | 微波使局部血液受热而使血液胶体凝固 | |
| C. | 微波电流通过手术刀时产生的高温使血液凝固 | |
| D. | 以上说法都正确 |
3.将一盛满Cl2的试管倒立在水槽,当日子照射相当长时间后,试管中剩余气体的体积约占试管容积的(假设反应前后体系温度相同)( )
| A. | $\frac{1}{4}$ | B. | $\frac{1}{3}$ | C. | $\frac{1}{2}$ | D. | $\frac{2}{3}$ |
 以天然气为原料合成甲醇常见的方法有水煤气法和目前正在开发的直接氧化法
以天然气为原料合成甲醇常见的方法有水煤气法和目前正在开发的直接氧化法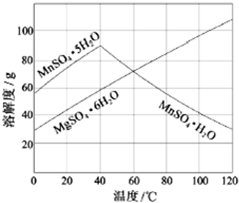 软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中SO2反应可制备MnSO4•H2O,反应的化学方程式为:MnO2+SO2═MnSO4.
软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中SO2反应可制备MnSO4•H2O,反应的化学方程式为:MnO2+SO2═MnSO4.