题目内容
2.化合物E是一种医药中间体,常用于制备抗凝血药,可以通过如图所示的路线合成: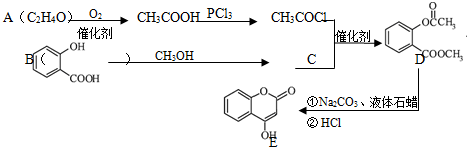
(1)A中含有的官能团名称为醛基.
(2)C转化为D的反应类型是取代反应.
(3)写出D与足量NaOH溶液完全反应的化学方程式
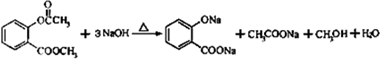 .
.(4)写出同时满足下列条件的B的一种同分异构体的结构简式
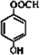 .
.A.能发生银镜反应. B.核磁共振氢谱只有4个峰.
C.能与FeCl3溶液发生显色反应,水解时每摩尔可消耗3摩尔NaOH.
(5)已知工业上以氯苯水解制取苯酚,而酚羟基一般不易直接与羧酸酯化.
苯甲酸苯酚酯
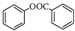 )是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选).合成路线流程图示例如下:
)是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选).合成路线流程图示例如下: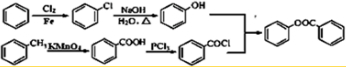 .
.H2C═CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH浓酸}$CH3CH2OH.
分析 由合成流程可知,A氧化得乙酸,所以A为CH3CHO,B为邻羟基苯甲酸发生酯化反应生成C,C为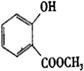 ,C与CH3COCl发生取代反应生成D,D中含-COOC-,能发生水解反应,D水解酸化后发生酯化反应生成E,以苯、甲苯为原料制取
,C与CH3COCl发生取代反应生成D,D中含-COOC-,能发生水解反应,D水解酸化后发生酯化反应生成E,以苯、甲苯为原料制取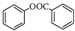 ,可以将甲苯氧化生成苯甲酸,苯甲酸再与三氯化磷反应生成苯甲酰氯,苯取代生成氯苯,水解生成苯酚,苯甲酰氯与苯酚发生取代反应得
,可以将甲苯氧化生成苯甲酸,苯甲酸再与三氯化磷反应生成苯甲酰氯,苯取代生成氯苯,水解生成苯酚,苯甲酰氯与苯酚发生取代反应得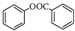 ,然后结合有机物的结构与性质来解答.
,然后结合有机物的结构与性质来解答.
解答 解:由合成流程可知,A氧化得乙酸,所以A为CH3CHO,B为邻羟基苯甲酸发生酯化反应生成C,C为 ,C与CH3COCl发生取代反应生成D,D中含-COOC-,能发生水解反应,D水解酸化后发生酯化反应生成E,
,C与CH3COCl发生取代反应生成D,D中含-COOC-,能发生水解反应,D水解酸化后发生酯化反应生成E,
(1)A为乙醛,含-CHO,名称为醛基,
故答案为:醛基;
(2)由上述分析可知,C中的-OH上的H被取代,则C转化为D的反应类型是取代反应,
故答案为:取代反应;
(3)D与足量NaOH溶液完全反应的化学方程式为 ,
,
故答案为: ;
;
(4)B为邻羟基苯甲酸,其同分异构体符合:
A.能够发生银镜反应,含-CHO;
B.核磁共振氢谱只有4个峰,含4种位置的H;
C.能与FeCl3溶液发生显色反应,含酚-OH,水解时每摩尔可消耗3摩尔NaOH,含-COOCH,所以同分异构体为 ,
,
故答案为: ;
;
(5)以苯、甲苯为原料制取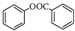 ,可以将甲苯氧化生成苯甲酸,苯甲酸再与三氯化磷反应生成苯甲酰氯,苯取代生成氯苯,水解生成苯酚,苯甲酰氯与苯酚发生取代反应得
,可以将甲苯氧化生成苯甲酸,苯甲酸再与三氯化磷反应生成苯甲酰氯,苯取代生成氯苯,水解生成苯酚,苯甲酰氯与苯酚发生取代反应得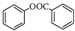 ,合成流程图为
,合成流程图为 ,
,
故答案为: .
.
点评 本题考查有机物的合成,为高考常见的题型,注意把握合成流程中的反应条件、已知信息等推断各物质,熟悉有机物的结构与性质即可解答,题目难度中等.

练习册系列答案
相关题目
13.设NA为阿佛加德罗常数,下列说法正确的是( )
①标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA
②同温同压下,体积相同的氢气和氩气所含的分子数相等
③1L 2mol/L的氯化镁溶液中含氯离子为4NA
④标准状况下22.4LH2O中分子数为NA
⑤32g O2和O3混合气体中含有原子数为2NA.
①标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA
②同温同压下,体积相同的氢气和氩气所含的分子数相等
③1L 2mol/L的氯化镁溶液中含氯离子为4NA
④标准状况下22.4LH2O中分子数为NA
⑤32g O2和O3混合气体中含有原子数为2NA.
| A. | ①②③④ | B. | ③④ | C. | ①③④ | D. | ①②③⑤ |
17.实验室区别下列物质选用的试剂(括号中的为试剂,必要时可加热)正确的是( )
| A. | 苯和己烷(溴水) | B. | 乙醛和丙烯酸(KMnO4溶液) | ||
| C. | 矿物油和植物油(NaOH溶液) | D. | 硝基苯和CCl4(水) |
14.在指定条件下,下列粒子一定能大量共存的是( )
| A. | 使酚酞变红色的溶液中:Na+、Fe3+、SO42-、Cl- | |
| B. | 饱和氯水中:K+、Na+、Cl-、HSO3- | |
| C. | 室温下,pH=13的溶液中:Na+、K+、SiO32-、Cl- | |
| D. | 1.0mol/L的KNO3溶液:H+、Fe2+、Cl-、SO32- |
11.今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、Al3+、Ba2+、SO42-、OH-,现取两份100mL该溶液进行如下实验:
(1)第一份加足量BaCl2溶液后,得干燥沉淀4.66g;
(2)第二份加NaOH溶液有沉淀产生,继续滴加至沉淀溶解,共消耗NaOH 0.04mol;
根据上述实验,以下推测正确的是( )
(1)第一份加足量BaCl2溶液后,得干燥沉淀4.66g;
(2)第二份加NaOH溶液有沉淀产生,继续滴加至沉淀溶解,共消耗NaOH 0.04mol;
根据上述实验,以下推测正确的是( )
| A. | C(SO42- )为0.02mol/L | B. | 100mL溶液中含有0.01mol Al3+ | ||
| C. | 溶液中一定存在Na+ | D. | 无法确定是否含有SO42- |
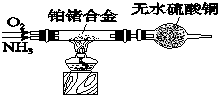 氮及其化合物在很多方面有重要的用途.
氮及其化合物在很多方面有重要的用途. .
.