题目内容
【题目】氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气燃烧热值高。实验测得,在常温常压下,1 g H2完全燃烧生成液态水,放出142.9 kJ热量。则H2燃烧的热化学方程式为__________________________________。
(2)氢氧燃料电池能量转化率高,具有广阔的发展前景。现氢氧燃料电池进行下图所示实验:①氢氧燃料电池中,正极的电极反应式为_____ _。
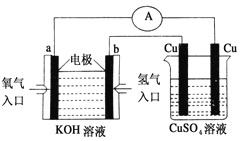
②如图装置中,某一铜电极的质量减轻3.2 g,则a极上消耗的O2在标准状况下的体积为____________L
(3)氢气是合成氨的重要原料,合成氨反应的热化方程式如下:N2(g)+3H2(g)![]() 2NH3(g);ΔH=-92.4 kJ/mol①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),
2NH3(g);ΔH=-92.4 kJ/mol①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),
反应速率与时间的关系如下图所示。
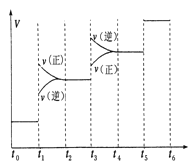
图中t1时引起平衡移动的条件可能是__________其中表示平衡混合物中NH3的含量最高的一段时间是_____
②温度为T ℃时,将2 a mol H2和a mol N2放入0.5 L密闭容器中,充分反应
后测得N2的转化率为50%。则反应的平衡常数为____________。
【答案】(1)2H2(g)+O2(g)=2H2O(l);ΔH=-571.6 kJ/mol;
(2)①O2+4e-+2H2O=4OH-;②0.56; (3)①增大压强;t2-t3;②![]() 。
。
【解析】
试题分析:(1)在298K、101kPa时,1g即0.5molH2完全燃烧生成液态水,放出142.9kJ热量,则表示H2燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol;(2)氢氧燃料电池能量转化率高,具有广阔的发展前景。现氢氧燃料电池进行下图所示实验:①在如图所示的氢氧燃料电池中,正极上氧气获得电子,由于溶液为碱性,所以氧气获得电子变为OH-,正极的电极反应式为O2+4e-+2H2O=4OH-;②根据如图装置可知与正极a连接的铜电极是阳极,发生氧化反应:Cu-2e-=Cu2+,质量减轻3.2 g,n(Cu)=3.2g÷64g/mol=0.05mol,则n(e-)=0.05mol×2=0.1mol,则a极上消耗的O2在标准状况下的体积为V(O2)= (0.1mol÷4) ×22.4L/mol=0.56L;①该反应的正反应是气体体积减小的放热反应。t1时刻,正逆速率都增大,正反应速率增大更多,平衡正向移动,正反应为气体体积减小的放热反应,升高温度平衡逆向移动,应是增大压强;t2-t3时反应处于平衡状态,从t3时刻开始化学平衡逆向移动,氨气的含量降低,在t4时达到平衡状态,从t4—t6时反应处于平衡状态。氨的含量不变。故表示平衡混合物中NH3的含量最高的一段时间是t2-t3;②温度为T℃时,将2a mol H2和a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%,氮气浓度变化量为(amol÷0.5L)×50%=amol/L,则:
N2(g)+3H2(g) ![]() 2NH3(g)
2NH3(g)
起始浓度(mol/L):2a 4a 0
变化浓度(mol/L):a 3a 2a
平衡浓度(mol/L):a a 2a
故平衡常数K=![]() 。
。