题目内容
6.已知实验室中,可用Co2O3代替MnO2来制备氯气,反应前后存在的六种微粒分别是:Co2O3、H2O、Cl2、H+、Cl-和Co2+.下列叙述不正确的是( )| A. | Cl2发生还原反应 | |
| B. | 氧化剂与还原剂的物质的量之比为1:2 | |
| C. | 若反应中生成3molH2O,则转移电子2mol | |
| D. | 理论上利用该反应可以将化学能转化为电能 |
分析 发生反应为Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O中,Co元素的化合价由+3价降低为+2价,Cl元素的化合价由-1价升高到0价,以此来解答.
解答 解:发生反应为Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O,
A.氯气为生成物,为氧化产物,故A错误;
B.6molHCl参加反应,只有2molHCl作还原剂,所以氧化剂与还原剂的物质的量之比为1:2,故B正确;
C.由反应及元素的化合价可知,生成3molH2O时转移的电子为2mol×(3-2)=2mol,故C正确;
D.为自发进行的氧化还原反应,可以将化学能转化为电能,故D正确.
故选A.
点评 本题考查氧化还原反应,为高考常见题型和高频考点,侧重于学生的分析能力的考查,明确元素的化合价变化及氧化还原反应中的概念即可解答,注意能写出反应的化学方程式或离子方程式,题目难度不大.

练习册系列答案
相关题目
16.反应2SO2+O2$?_{△}^{催化剂}$2SO3经一段时间后,SO3的浓度增加了0.8mol•L-1,在这段时间内用O2表示的反应速率为0.04mol•L-1•s-1,则这段时间为( )
| A. | 0.1 s | B. | 2.5 s | C. | 5 s | D. | 10 s |
14.用水稀释0.1mol/L的醋酸溶液,其中随加水量的增加而增大的有( )
①n(H+) ②c(H+) ③c(H+)/c(CH3COOH)④c(CH3COOH)/c(H+)
①n(H+) ②c(H+) ③c(H+)/c(CH3COOH)④c(CH3COOH)/c(H+)
| A. | ①④ | B. | ②③ | C. | ②④ | D. | ①③ |
11.下列可以大量共存且溶液为无色的离子组是( )
| A. | H+、Na+、NO3-、MnO4- | B. | Fe2+、Ba2+、Cl-、SO42- | ||
| C. | Na+、K+、Cu2+、NO3- | D. | NO3-、SO42-、K+、Na+ |
15.分子式为C2H402且可与Na0H溶液反应的有机化合物有( )
| A. | 5种 | B. | 6种 | C. | 2种 | D. | 8种 |
11.下列物质属于能导电的强电解质的是( )
| A. | 醋酸 | B. | 氯化钠溶液 | C. | 乙醇 | D. | 熔融的硫酸钡 |
 铝的阳极氧化,是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜.某化学研究小组在实验室中按下列步骤模拟该生产过程,装置如图.填写下列空白:
铝的阳极氧化,是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜.某化学研究小组在实验室中按下列步骤模拟该生产过程,装置如图.填写下列空白: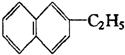 属于萘的同系物,则萘和萘的同系物分子组成通式为CnH2n-12 (n≥10).
属于萘的同系物,则萘和萘的同系物分子组成通式为CnH2n-12 (n≥10).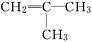 ②丙的结构简式为
②丙的结构简式为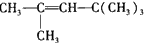 .
.