题目内容
【题目】某研究性学习小组设计了如图装置制取和验证SO2的性质。
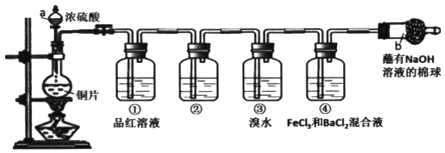
请回答:
(1)写出图中仪器的名称:a________,b________。
(2)棉球中NaOH溶液的作用是________。
(3)为了验证SO2是酸性氧化物,洗气瓶②中可选择的试剂是_______。
A 紫色石蕊试液 B 无色酚酞试液 C 澄清石灰水 D 碘水
(4)下列说法正确的是_______。
A 实验开始时,只需打开分液漏斗的旋塞,即可使液体顺利滴下
B 先向装置中加入试剂(药品),再进行气密性检查
C 实验开始后,洗气瓶①和③中溶液均褪色,两者均可证明SO2具有漂白性
D 实验开始后,洗气瓶④中可观察到白色沉淀产生,该现象可说明SO2具有还原性
【答案】分液漏斗 干燥管 吸收尾气,防止SO2污染大气 AC D
【解析】
在加热的条件下铜和浓硫酸反应生成二氧化硫,二氧化硫具有漂白性能使品红溶液褪色,具有还原性能被溴水和氯化铁溶液氧化,最后进行尾气处理,据此分析解答。
(1)图示仪器a为分液漏斗;图示仪器b为干燥管;
(2)二氧化硫有毒,是大气污染物,干燥管为尾气吸收装置,其中的NaOH是用于吸收过量的SO2,防止造成空气污染;
(3)A、SO2通入紫色石蕊试液中,溶液变红色,说明SO2能与水反应形成酸,A符合题意;
B、SO2通入无色酚酞溶液中,溶液不变色,B不符合题意;
C、SO2通入澄清石灰水中,溶液变浑浊,说明SO2能与碱反应,C符合题意;
D、SO2通入碘水中,碘水褪色,说明二者发生反应,体现二氧化硫的还原性,但不能说明SO2是酸性氧化物,D不符合题意;
故答案为:AC。
(4)A、实验开始时,应先打开分液漏斗上口的瓶塞,再打开分液漏斗的旋塞,液体才能顺利滴下,选项错误,A不符合题意;
B、实验开始前,应先检查装置的气密性,再加入药品,选项错误,B不符合题意;
C、洗气瓶①中品红溶液褪色,体现了SO2的漂白性;洗气瓶③中溴水褪色,发生了反应:Br2+SO2+2H2O=2HBr+H2SO4,体现了SO2的还原性,选项错误,C不符合题意;
D、洗气瓶④中产生的白色沉淀为BaSO4,SO42-是SO2被Fe3+氧化而来的,体现了SO2的还原性,选项正确,D符合题意;
故答案为:D。

 名校课堂系列答案
名校课堂系列答案【题目】在一体积2L的密闭容器中加入反应物N2、H2,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g)。反应过程中的部分数据如下表所示,下列说法正确的是
2NH3(g)。反应过程中的部分数据如下表所示,下列说法正确的是
物质的量/ mol 时间/min | n(N2) | n(H2) | n(NH3) |
0 | 1.0 | 1.2 | 0 |
2 | 0.9 | ||
4 | 0.75 | ||
6 | 0.3 |
A. 0~2 min内,NH3的反应速率为0.1 mol·Lˉ1·minˉ1
B. 2 min时, H2的物质的量0.3 mol
C. 4 min时,反应已达到平衡状态,此时正、逆反应的速率都为0
D. 4~6 min内,容器内气体分子的总物质的量不变
【题目】电镀行业中废水处理后产生的含重金属污泥废弃物称为电镀污泥,被列入国家危险废物名单中的第十七类危险废物。工业上可利用某电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等金金属,其利用回收流程如下:

已知部分物质沉淀的pH及CaSO4的溶解度曲线如下:
Fe3+ | Cu2+ | Cr3+ | |
开始沉淀的pH | 2.1 | 4.7 | 4.3 |
恰好完全沉淀的pH | 3.2 | 6.7 | a |

(1)浸出过程中的生成物主要是Fe2(SO4)3和_______________(填化学式)
(2)除铁等相关操作:
①加入石灰乳调节pH应满足要求是_______________;
②将浊液加热到80℃,趁热过滤。滤渣Ⅱ的主要成分是______________(填化学式)。
(3)还原步骤中生成Cu2O固体的离子反应方程式______________,此步骤中加入NaHSO3的不能过量______________ (离子方程式表达)。
(4)当离子浓度≤1×10-5mol·L-1时认为沉淀完全,则表格中a的值是______________。(已知:T=25℃,Ksp[Cr(OH)3]=6.3×10-31,![]() ,lg2=0.3)
,lg2=0.3)
(5)将铬块加入到稀盐酸或稀硫酸中,可观察到铬逐渐溶解,同时放出氢气。但若将铬块加稀硝酸中,却看不到明显现象。由此推测,出现该现象的可能原因是____________________________。
(6)处理大量低浓度的含铬废水(以CrO42-计)可采用离子交换法,其原理是采用季胺型强碱性阴离子交换树脂(RN—OH),使庞水中CrO42-与树脂上的OH发生离子交换反应。一段时间后停lh 通废水,再通NaOH溶液时CrO42-进入溶液回收,并使树脂得到再生。请用离子方程式表示该交换过程____________。


