题目内容
【题目】如图所示的C-NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍。该电池反应式为:NaMO2+nC![]() Na(1-x)MO2+NaxCn,下列正确的是
Na(1-x)MO2+NaxCn,下列正确的是

A. 充电时,左侧电极为阳极
B. 电解质可以选用无水乙醇
C. 放电时,负极电极反应时为:NaMO2-xe-=Na(1-x)MO2+xNa+
D. 充电时,阳极电极反应式为:nC+xNa-xe-=NaxCn
【答案】C
【解析】
A、充电时,钠离子移向左侧,左侧电极为阴极;
B、无水乙醇为非电解质;
C、原电池中,负极发生失电子的氧化反应;
D、电解池中,阳极上发生失电子的氧化反应;
A、充电时,钠离子移向左侧,左侧电极为阴极,故A错误;
B、无水乙醇为非电解质,不能电离,不导电,故B错误;
C、原电池中,负极发生失电子的氧化反应:放电时,负极电极反应时为:NaMO2-xe-=Na(1-x)MO2+xNa+,故C正确;
D、电解池中,阳极上发生失电子的氧化反应:电极反应式为NaxCn-xe-═nC+x Na+,故D错误。
故选C。

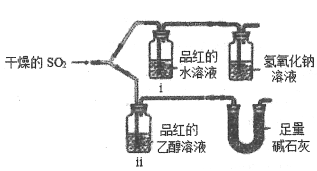
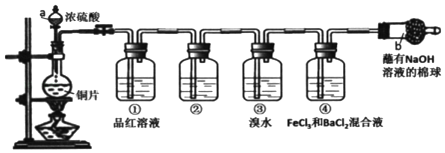
【题目】如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。

(1)检查装置 A 的气密性方法是:_____。
(2)装置 B 中饱和食盐水的作用是_____;同时装置 B 亦是安全瓶,监测实验进行时 C中是否发生堵塞,请写出发生堵塞时 B 中的现象_____。
(3)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ依次放入_____。
A | B | C | D | |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)设计装置 D、E 的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置 D 中少量溶液加入装置 E 中,振荡,观察到的现象是_____,该现 象_____(填“能”或“不能”)说明溴单质的氧化性强于碘,原因是_____。