题目内容
已知在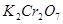 的溶液中存在着如下平衡:
的溶液中存在着如下平衡: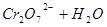
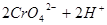 加入下列物质能使溶液变为橙色的是
加入下列物质能使溶液变为橙色的是
(橙色) (黄色)
| A.氨水 | B.硫酸 | C.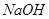 | D.水 |
B
解析试题分析:由于该反应是可逆反应,要使溶液变为橙色,也就是使平衡向逆反应方向移动。根据平衡移动原理:增大生成物的浓度如增大溶液的c(H+)平衡向逆向移动,溶液的橙色加深,故选项是B。
考点:考查影响化学平衡移动的因素的知识。

练习册系列答案
相关题目
t℃时,在体积不变的容器中发生反应X(g)+3Y(g) 2Z(g)△H<O各组分浓度如下表
2Z(g)△H<O各组分浓度如下表
| 物质 | X | Y | Z |
| 初始浓度/ mol·L-1 | 0.1 | 0.3 | 0 |
| 2min末浓度/mol·L-1 | 0.08 | | |
| 平衡浓度/mol·L-1 | | | 0.1 |
A .0~2min的平均速率v(x) ="0." 01 mol·L-1·min-1
B.达平衡时Y的转化率为50%
C.其它条件不变,升高温度,平衡逆向移动
D.其它条件不变,增加X的浓度,ν正增大
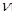 逆碱小,平衡正向移动
逆碱小,平衡正向移动 已知有反应:I2(g)+H2(g)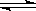 2HI(g)△H<0,该反应在恒容的密闭容器中达到平衡后,若仅改变图中x的值,则y随x变化趋势合理的是
2HI(g)△H<0,该反应在恒容的密闭容器中达到平衡后,若仅改变图中x的值,则y随x变化趋势合理的是
| 选项 | X | Y | 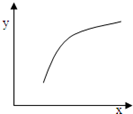 |
| A | 温度 | 容器内混合气体的密度 | |
| B | I2的物质的量 | H2的转化率 | |
| C | H2的浓度 | 平衡常数K | |
| D | 加入Ar的物质的量 | 逆反应速率 |
下图为某化学反应速率-时间图。在t1时刻升高温度或增大压强,都符合下图所示变化的反应是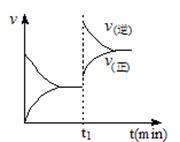
A.2SO2(g)+O2(g) 2SO3(g) △H<0 2SO3(g) △H<0 |
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H<0 4NO(g)+6H2O(g) △H<0 |
C.H2(g)+I2(g) 2HI(g) △H>0 2HI(g) △H>0 |
D.C(s)+H2O(g) CO(g)+H2(g) △H>0 CO(g)+H2(g) △H>0 |
已知某反应aA(g)+bB(g)?==?cC(g)的各物质浓度数据如下:
| | A | B | C |
| 起始浓度(mol·L-1) | 3.0 | 1.0 | 0 |
| 2 s末浓度(mol·L-1) | 1.8 | 0.6 | 0.8 |
A.9∶3∶4 B.3∶1∶2 C.2∶1∶3 D.3∶2∶1
工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+ O2 2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是( )
2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是( )
| A.使用催化剂是为了加快反应速率,提高生产效率 |
| B.在上述条件下,SO2不可能100%地转化为SO3 |
| C.为了提高SO2的转化率,应适当提高O2的浓度 |
| D.达到平衡时,SO2的浓度与SO3的浓度相等 |
在恒温密闭容器中进行反应N2(g) + O2(g) = 2NO(g),下列反应措施能加快反应速率的是
| A.缩小体积使压强增大 | B.压强不变,充入N2使体积增大 |
| C.体积不变,充入He使压强增大 | D.压强不变,充入He使体积增大 |
如图为某化学反应的速率与时间的关系示意图。在t1时刻升高温度或增大压强,速率的变化都符合示意图的反应是: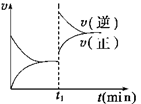
A.2A(g) + B(g) 2C(g) ΔH>0 2C(g) ΔH>0 |
B.2SO2(g)+ O2(g)  2SO3(g)ΔH<0 2SO3(g)ΔH<0 |
C.H2(g) + I2(g)  2HI(g)ΔH>0 2HI(g)ΔH>0 |
D.4NH3(g)+ 5O2(g)  4NO(g) + 6H2O(g)ΔH<0 4NO(g) + 6H2O(g)ΔH<0 |