题目内容
【题目】下列实验操作都能够达到预期目的是
A.用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸,并测得某溶液pH为![]()
B.中和pH与体积均相同的NaOH溶液和氨水,结果消耗![]() 的物质的量一样多
的物质的量一样多
C.酸碱中和滴定的终点是指酸和碱恰好完全反应,此时溶液一定呈中性
D.在HCl气氛中蒸干![]() 溶液能到得纯净的无水氯化铝
溶液能到得纯净的无水氯化铝
【答案】D
【解析】
A.水湿润pH试纸,稀释了待测溶液,使溶液的酸碱性减弱,若测定的是酸性溶液,则会使测定结果变大;若测定的是碱性溶液,则会使测定结果变小;若测定的是中性溶液,则会使测定结果不变,且测得值只能是整数,故A错误;
B.一水合氨是弱电解质,NaOH是强电解质,相同温度下pH相等的氢氧化钠和氨水溶液,氨水浓度大于NaOH,根据![]() 知,两种溶液中溶质的物质的量不等,所以消耗硫酸的物质的量不等,故B错误;
知,两种溶液中溶质的物质的量不等,所以消耗硫酸的物质的量不等,故B错误;
C.酸和碱恰好完全反应,若是强酸强碱反应,溶液呈中性,若是强酸弱碱反应,溶液呈酸性,若是弱酸强碱反应溶液呈碱性,故C错误;
D.![]() 加热水解生成
加热水解生成![]() ,在HCl气氛中蒸干
,在HCl气氛中蒸干![]() 溶液抑制铝离子水解,能到得纯净的无水氯化铝,故D正确.
溶液抑制铝离子水解,能到得纯净的无水氯化铝,故D正确.
故选D。

 阅读快车系列答案
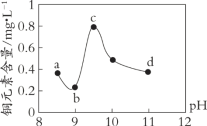
阅读快车系列答案【题目】某电路板生产企业的水质情况及国家允许排放的污水标准如下表所示。为研究废水中Cu2+处理的最佳pH,取5份等量的废水,分别用30%的NaOH溶液调节pH至8.5、9、9.5、10、11,静置后,分析上层清液中铜元素的含量,实验结果如下图所示。
查阅资料,平衡I:Cu(OH)2 + 4NH3 ![]() [Cu(NH3)4]2+ + 2OH-;
[Cu(NH3)4]2+ + 2OH-;
平衡II:Cu(OH)2 + 2OH- ![]() [Cu(OH-)4]2-
[Cu(OH-)4]2-
项目 | 废水水质 | 排放标准 |
pH | 1.0 | 6~9 |
Cu2+/ mg·L-1 | 72 | ≤0.5 |
NH4+/ mg·L-1 | 2632 | ≤15 |
下列说法不正确的是
A. 废水中Cu2+处理的最佳pH约为9
B. b~c段:随pH升高,Cu(OH)2的量增加,平衡I正向移动,铜元素含量上升
C. c~d段:随pH升高,c(OH-)增加,平衡I逆向移动,铜元素含量下降
D. d点以后,随c(OH-)增加,铜元素含量可能上升