题目内容
【题目】下列关于化学反应的图像的说法不正确是 ( )
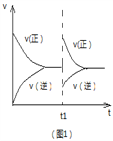
A. 图1可表示反应2NO2![]() N2O4 在等温等压条件下平衡后t1时刻充入NO2时反应速率变化
N2O4 在等温等压条件下平衡后t1时刻充入NO2时反应速率变化
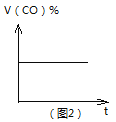
B. 图2可表示CO(g)+2H2(g)![]() CH3OH(g)在一定温度下,将0.5mol CO和0.5mol H2在体积为2L的密闭容器中发生反应时CO的体积分数随时间变化图像。
CH3OH(g)在一定温度下,将0.5mol CO和0.5mol H2在体积为2L的密闭容器中发生反应时CO的体积分数随时间变化图像。
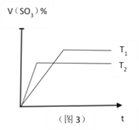
C. 图3可表示反应2SO2 +O2![]() 2SO3 ,温度T1>T2,反应为吸热反应。
2SO3 ,温度T1>T2,反应为吸热反应。
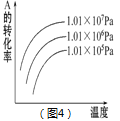
D. 图4可表示反应mA(g)+nB(g)![]() pC(g)+qD(g),正反应是吸热反应,且m+n>p+q。
pC(g)+qD(g),正反应是吸热反应,且m+n>p+q。
【答案】C
【解析】A. 在等温等压条件下,平衡后t1时刻充入NO2,正反应速率增大,逆反应速率减小,最后重新达到平衡状态,故A正确;B. 将0.5mol CO和0.5mol H2在体积为2L的密闭容器中发生反应,起始时CO与H2的体积比为1:1,CO的体积分数为50%,设反应过程中CO消耗xmol,则:
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
起始(mol) 0.5 0.5 0
转化(mol) x 2x x
则CO的体积分数为: ![]() ×100% =
×100% =![]() ×100%=50%,所以在反应过程中CO的体积分数不变,故B正确;C. 根据“先拐先平数值大”的原则,温度T2>T1,温度高时SO3的体积分数小,说明升高温度平衡逆向移动,则正反应为放热反应,故C错误;D. 由图可知,升高温度,A的转化率增大,说明升高温度平衡正向移动,正反应为吸热反应,压强越大,A的转化率越大,说明增大压强,平衡正向移动,正反应方向为气体减少的方向,则m+n>p+q,故D正确;答案选C。
×100%=50%,所以在反应过程中CO的体积分数不变,故B正确;C. 根据“先拐先平数值大”的原则,温度T2>T1,温度高时SO3的体积分数小,说明升高温度平衡逆向移动,则正反应为放热反应,故C错误;D. 由图可知,升高温度,A的转化率增大,说明升高温度平衡正向移动,正反应为吸热反应,压强越大,A的转化率越大,说明增大压强,平衡正向移动,正反应方向为气体减少的方向,则m+n>p+q,故D正确;答案选C。

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目