题目内容
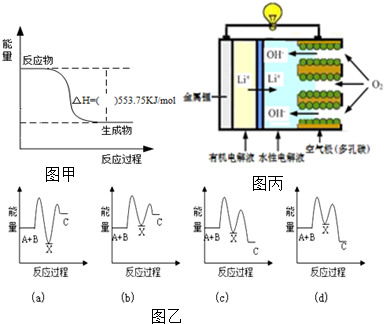
7. 下列各种说法或表述正确的是⑤⑥.
下列各种说法或表述正确的是⑤⑥.①石油、煤、天然气、可燃冰、植物油都属于化石燃料.
②开发核能、太阳能等新能源,推广甲醇汽油,使用无磷洗涤剂都可直接降低碳排放
③甲烷的燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为
CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ/mol
④500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:
N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ/mol
⑤利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学方法
⑥已知:S(g)+O2(g)=SO2(g)△H1<0 S(s)+O2(g)=SO2(g)△H2<0
则有:△H1<△H2.
分析 ①石油、煤、天然气、可燃冰为化石燃料;
②根据无磷洗涤剂的成分来回答;
③燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量分析;
④0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,生成的氨气的物质的量小于1mol;
⑤利用太阳能和催化剂分解水没有污染;
⑥固体硫转化为气态硫的过程是吸热的过程.
解答 解:①石油、煤、天然气、可燃冰为化石燃料,而植物油不属于化石燃料,故错误;
②无磷洗涤剂是在洗涤剂的成分中去掉了导致水污染的磷元素,它不会降低碳排放,故错误;
③根据燃烧热的概念:1mol可燃物完全燃烧生成稳定的氧化物,所放出的热量为燃烧热,水的状态应该为液态,故错误;
④0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,因反应为可逆反应,则1molN2和3molH2置于密闭的容器中充分反应生成NH3(g),放热不是38.6kJ,则热化学反应方程式中的反应热数值错误,故错误;
⑤利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能,不消耗能源,也不产生污染,是一种绿色化学方法,故正确;
⑥固体硫转化为气态硫的过程是吸热的过程,所以等量的气态硫燃烧放热多,即:△H1<△H2,故正确.
故选⑤⑥.
点评 本题考查学生反应热的有关知识,注意对中和热和燃烧热的概念理解,掌握基础是关键,题目难度不大.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
20.选择合适试剂完成甲、乙两组实验.
甲组:检验含Fe3+的溶液中是否含有Fe2+;
乙组:检验含Fe2+的溶液中是否含有Fe3+.
下列试剂及加入试剂顺序能达到实验目的是( )
甲组:检验含Fe3+的溶液中是否含有Fe2+;
乙组:检验含Fe2+的溶液中是否含有Fe3+.
下列试剂及加入试剂顺序能达到实验目的是( )
| 试剂 选项 | 甲组 | 乙组 |
| A | 新制氯水、KSCN溶液 | NaOH溶液 |
| B | 酸性KmnO4溶液 | KSCN溶液 |
| C | KOH溶液 | 溴水 |
| D | 溴水 | 酸性KmnO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
2.某温度下,反应2SO2(g)+O2(g)═2SO3 (g) 的平衡常数K1=25,在同一温度下,反应SO3(g)═SO2(g)+$\frac{1}{2}$O2(g)的平衡常数K2的值为( )
| A. | 50 | B. | 5 | C. | 0.2 | D. | 0.01 |
12.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,则含40.0gNaOH的稀溶液与足量稀醋酸完全中和,放出的热量小于57.3kJ | |
| B. | 2C(s)+2O2(g)═2CO2(g)△H=akJ•mol-1:2C(s)+O2(g)═2CO(g)△H=bkJ•mol-1,则a>b | |
| C. | 氢气的燃烧热为285.5 kJ•mol-1,则水分解的热化学方程式为:2H2O(l)═2H2(g)+O2(g);△H=+285.5 kJ•mol-1 | |
| D. | 已知正丁烷(g)→异丁烷(g)△H<0,则正丁烷比异丁烷稳定 |
19.在下列各溶液中,离子一定能大量共存的是( )
| A. | 强碱性无色溶液中:K+、Fe3+、Cl-、SO42- | |
| B. | 滴加石蕊试液显红色的溶液:K+、Mg2+、Cl-、NO3- | |
| C. | 含有0.1mol•L-1Ca2+的溶液中:Na+、K+、CO32-、Cl- | |
| D. | 滴加酚酞试液显红色的溶液:Ba2+、H+、NO3-、Cl- |
16.实验室有两瓶失去标签的溶液,其中一瓶是H2SO4,另一瓶是蔗糖溶液.鉴别时,下列选用的试纸或试剂不正确的是( )
| A. | pH试纸 | B. | KCl溶液 | C. | BaCl2溶液 | D. | Na2CO3溶液 |