题目内容
19.由H2SO4、Al2O3、NaOH、Mg、Cl2两两之间可进行反应,可生成正盐.试回答:能生成正盐的化学式有(写六种)Al2(SO4)3、Na2SO4、MgSO4、NaAlO2、MgCl2、NaCl、NaClO.分析 利用所学的化学反应知识结合复分解反应的发生条件,对所给物质进行两两组合找到反应的产物即可.
解答 解:从五种物质中任意选出两种反应,一一分析即可:
H2SO4与Al2O3反应生成正盐Al2(SO4)3;
H2SO4与NaOH反应生成正盐Na2SO4;
H2SO4与Mg反应生成正盐MgSO4;
Al2O3与NaOH反应生成正盐NaAlO2;
NaOH与Cl2反应生成NaCl和NaClO都是正盐;
Mg与Cl2反应生成正盐MgCl2,
故答案为:Al2(SO4)3、Na2SO4、MgSO4、NaAlO2、MgCl2、NaCl、NaClO.
点评 此题是对物质间反应的考查,解题的关键是对各物质性质的了解,同时还要结合复分解反应的发生条件以及金属与盐溶液的反应规律进行判断.

练习册系列答案
相关题目
9.一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)$\stackrel{催化剂}{?}$2CO2(g)+S(1)△H<0.若反应在恒容的密闭容器中进行,下列有关说法不正确的是( )
| A. | 其它条件不变,使用不同催化剂,该反应的平衡常数不变 | |
| B. | 平衡前,随着反应的进行,容器内压强始终不变 | |
| C. | 平衡时,其它条件不变,分离出少量的硫,正反应速率不变 | |
| D. | 平衡时,其他条件不变,升高温度可使反应速率加快,平衡常数减小 |
10.下列事实中,不能用平衡移动原理解释的是( )
| A. | 工业上合成氨,及时分离出产物氨有利于提高氮气的转化率 | |
| B. | 实验室中常用排饱和食盐水的方法收集氯气 | |
| C. | 由H2、I2(g)、HI组成的平衡体系,加压后颜色加深 | |
| D. | 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
7.不是构成原电池必需具备的条件是( )
| A. | 活泼性不同的两极 | B. | 闭合回路 | ||
| C. | 电源 | D. | 电解质溶液 |
14.下列离子方程式书写正确的是( )
| A. | 向碳酸氢钠溶液中滴加少量氢氧化钡溶液:2HCO-3+Ba2++2OH-═BaCO3↓+CO2-3+2H2O | |
| B. | 氢氧化钡溶液与稀硫酸混合:Ba2++SO2-4═BaSO4↓ | |
| C. | 氯气跟水反应:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 用氨水吸收少量二氧化碳:NH3•H2O+SO2═NH+4+HSO3- |
11.将由4.2g碳酸氢钠固体与5.8g氢氧化钠固体组成的混合物物在试管中加热,产生的气体通入澄清石灰水中,直至试管中固体质量不再变化得到固体A,则下列说法正确的是( )
| A. | 固体A中只含有氢氧化钠 | B. | 固体A中含有碳酸氢钠 | ||
| C. | 固体A中只含有碳酸钠 | D. | 固体A的质量为9.1g |

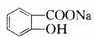 B
B D
D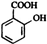 .写出D→E的反应的化学方程式
.写出D→E的反应的化学方程式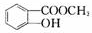 +H2O.
+H2O.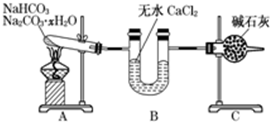
 下列各种说法或表述正确的是⑤⑥.
下列各种说法或表述正确的是⑤⑥.