题目内容
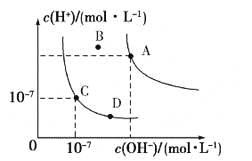
【题目】25℃时,将浓度均为0.1 mol·L-1,体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100 mL,Va、Vb与混合液pH的关系如图所示,下列说法正确的是
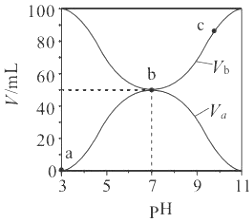
A. Ka(HA)=1×10-6
B. b点c(B+)=c(A-)=c(OH-)=c(H+)
C. a→c过程中水的电离程度始终增大
D. c点时,c(A-)/[c(OH-)c(HA)]随温度升高而减小
【答案】D
【解析】
根据图知,酸溶液的pH=3,则c(H+)<0.1mol/L,说明HA是弱酸;碱溶液的pH=11,c(OH-)<0.1mol/L,则BOH是弱碱,结合图像分析解答。
A、由图可知0.1mol/L HA溶液的pH=3,根据HAH++A-可知Ka=10-3×10-3/0.1=10-5,A错误;
B、b点是两者等体积混合溶液呈中性,所以离子浓度的大小为:c(B+)=c(A-)>c(H+)=c(OH-),B错误;
C、a→b是酸过量和b→c是碱过量两过程中水的电离程受抑制,b点是弱酸弱碱盐水解对水的电离起促进作用,所以a→c过程中水的电离程度先增大后减小,C错误;
D、c点时,c(A-)/[c(OH-)c(HA)]=1/Kh,水解平衡常数Kh只与温度有关,温度升高,Kh增大,1/Kh减小,所以c(A-)/[c(OH-)c(HA)]随温度升高而减小,D正确;
答案选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目