题目内容
在10 L密闭容器中,1 mol A和3 mol B在一定条件下反应:A(气)+xB(气) 2C(气),2min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是( )
2C(气),2min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是( )
 2C(气),2min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是( )
2C(气),2min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是( )| A.平衡时,物质的量比A∶B∶C=2∶11∶4 |
| B.x值等于4 |
| C.B的平均反应速率为0.04 mol·L-1·min-1 |
| D.A的转化率20% |
A
试题分析:根据反应方程式可知:0.4 mol C,则消耗0.2mol的A,消耗0.2X的B,剩余的A为(1-0.2)mol,B为(3-0.2X)mol,解得X=4,平衡时,物质的量比A∶B∶C=0.8∶1.4∶0.4=4:7:2. B的反应速率为(0.2mol×4)÷10L÷2min=0.04mol/(L·min).A的转化率为0.2mol÷1mol×100%=20%.因此计算结果不正确的是A。

练习册系列答案
相关题目
 2XY3(g)。图Ⅰ表示在一定温度下此反应过程中的能量变化;图Ⅱ表示在2 L的密闭容器中反应时X2的物质的量随时间的变化曲线;图Ⅲ表示在其他条件不变的情况下,改变起始物Y2的物质的量对此反应平衡的影响。
2XY3(g)。图Ⅰ表示在一定温度下此反应过程中的能量变化;图Ⅱ表示在2 L的密闭容器中反应时X2的物质的量随时间的变化曲线;图Ⅲ表示在其他条件不变的情况下,改变起始物Y2的物质的量对此反应平衡的影响。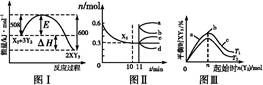
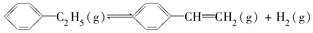 ΔH=a kJ·mol-1。经一段时间后达到平衡。反应过程中测定的部分数据见下表:
ΔH=a kJ·mol-1。经一段时间后达到平衡。反应过程中测定的部分数据见下表: 2NH3(g)。在相同时间内表示该反应速率最快的是
2NH3(g)。在相同时间内表示该反应速率最快的是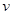 (W)=3
(W)=3 2SO3(g)(正反应放热)。测得n(O2)随时间的变化如下表
2SO3(g)(正反应放热)。测得n(O2)随时间的变化如下表