题目内容
2.填写下列表格:| 物质 | 指定的微粒/个 | 质量(m)g | 物质的量(n)mol | 摩尔质量(M)g/mol |
| He | 0.2 | |||
| S | 1.204×1023 | |||
| Na+ | 11.5 | |||
| C6H12O6 | 0.25 |
分析 摩尔质量以g/mol为单位,数值上等于其相对分子质量质量;
根据N=nNA计算氦气分子数目,根据m=nM计算He的质量;
根据n=$\frac{N}{{N}_{A}}$计算硫的物质的量,根据m=nM计算硫的质量;
根据n=$\frac{m}{M}$计算Na+的物质的量,根据N=nNA计算Na+离子数目,根据m=nM计算Na+的质量;
根据N=nNA计算C6H12O6分子数目,根据m=nM计算C6H12O6的质量.
解答 解:0.2molHe的分子数目为0.2mol×6.02×1023mol-1=1.204×1023,摩尔质量为4g/mol,其质量为0.2mol×4g/mol=0.8g;
1.204×1023个S原子物质的量为$\frac{1.204×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=0.2mol,其摩尔质量为32g/mol,质量为0.2mol×32g/mol=6.4g;
Na+的摩尔质量为23g/mol,11.5gNa+的物质的量为$\frac{11.5g}{23g/mol}$=0.5mol,Na+离子数目为0.5mol×6.02×1023mol-1=3.01×1023;
0.25mol C6H12O6的微粒数目为0.25mol×6.02×1023mol-1=1.505×1023,其摩尔质量为180g/mol,质量为0.25mol×180g/mol=45g,
故答案为:
| 物质 | 指定的微粒/个 | 质量(m)g | 物质的量(n)mol | 摩尔质量(M)g/mol |
| He | 1.204×1023 | 0.8 | 0.2 | 4 |
| S | 1.204×1023 | 6.4 | 0.2 | 32 |
| Na+ | 3.01×1023 | 11.5 | 0.5 | 23 |
| C6H12O6 | 1.505×1023 | 45 | 0.25 | 180 |
点评 本题考查物质的量有关计算,比较基础,注意掌握以物质的量为中心的有关计算.

练习册系列答案
相关题目
12.乙酸具有的官能团是( )
| A. | 碳碳双键 | B. | 羟基 | C. | 醛基 | D. | 羧基 |
13.下列叙述错误的是( )
| A. | 吸热反应的反应物总能量低于生成物总能量 | |
| B. | 绿色植物进行光合作用时,将光能转化为化学能“贮存”起来 | |
| C. | 电力属于一次能源 | |
| D. | 物质的化学能可以在不同条件下转为热能、电能、光能等为人类所利用 |
10.在①钾盐 ②铵盐 ③硝酸盐 ④硫酸盐 ⑤盐酸盐 ⑥碳酸盐中,均能溶于水的一组盐是( )
| A. | ①②⑤ | B. | ②③④ | C. | ①②③ | D. | ①③⑥ |
14.下列离子方程式正确的是( )
| A. | NaHSO3溶液与NaOH溶液反应:HSO${\;}_{3}^{-}$+OH-=SO${\;}_{3}^{2-}$+H2O | |
| B. | 少量二氧化碳通入足量的NaOH溶液:CO2+OH-=HCO${\;}_{3}^{-}$ | |
| C. | Fe与盐酸反应产生H2:2Fe+6H+=2Fe3++3H2↑ | |
| D. | 氨水和醋酸溶液混合NH3•H2O+CH3COOH=NH${\;}_{4}^{+}$+H2O |
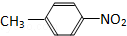 和
和
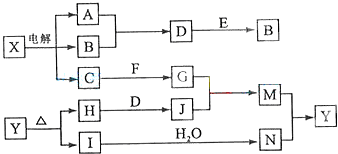
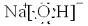 .
.