题目内容
【题目】在一定条件下,充分燃烧一定量的丁烷放出热量为Q kJ(Q>0),经测定完全吸收生成的CO2需消耗 5 mol·L-1的KOH溶液100 mL,恰好生成正盐,则此条件下反应C4H10(g)+O2(g)===4CO2(g)+5H2O(g)的ΔH为
A.+8Q kJ·mol-1 B. -16Q kJ·mol-1
C.-8Q kJ·mol-1 D. +16Q kJ·mol-1
【答案】B
【解析】
试题解析:KOH的物质的量为n(KOH)=c×V=0.1L×5mol/L=0.5mol,2KOH+CO2═K2CO3+H2O,根据钾离子守恒,故n(K2CO3)=0.5mol×![]() =0.25mol,根据碳元素守恒由n(CO2)=n(K2CO3)=0.25mol,
=0.25mol,根据碳元素守恒由n(CO2)=n(K2CO3)=0.25mol,
2C4H10+13O2![]() 8CO2+10H2O根据碳元素守恒可知,丁烷的物质的量为n(C4H10)=0.25mol×
8CO2+10H2O根据碳元素守恒可知,丁烷的物质的量为n(C4H10)=0.25mol×![]() =
=![]() mol,
mol,
即 ![]() mol丁烷放出的热量大小为QkJ,故1mol丁烷完全燃烧放出的热量为QkJ×
mol丁烷放出的热量大小为QkJ,故1mol丁烷完全燃烧放出的热量为QkJ×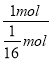 =16QkJ,
=16QkJ,
则此条件下反应热化学方程式为C4H10(g)+![]() O2(g)═4CO2(g)+5H2O(l)△H=-16Q kJmol-1.
O2(g)═4CO2(g)+5H2O(l)△H=-16Q kJmol-1.

练习册系列答案
相关题目