题目内容
(1)25℃时,浓度为0.1 mol·L-1的6种溶液:①HCl, ②CH3OOH, ③Ba(OH)2,④Na 2CO3,⑤KCl,⑥NH4Cl溶液pH由小到大的顺序为__________________(填写编号)。
(2)25℃时,醋酸的电离常数Ka=1.7×10-5mol/L,则该温度下CH3COONa的水解平衡常数Kh= mol ·L-1(保留到小数点后一位)。
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液呈 (填“酸性”,“中性”或“碱性”) ,请写出溶液中离子浓度间的一个等式: 。
(4)25℃时,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后,溶液的pH=7,
则溶液中c(CH3COO-) + c(CH3COOH)= ,m与n的大小关系是m n(填“ >”“=”或“<”)。
(5)25℃时,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的pH=7 ,则NH3·H2O的电离常数Ka= 。
(2)25℃时,醋酸的电离常数Ka=1.7×10-5mol/L,则该温度下CH3COONa的水解平衡常数Kh= mol ·L-1(保留到小数点后一位)。
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液呈 (填“酸性”,“中性”或“碱性”) ,请写出溶液中离子浓度间的一个等式: 。
(4)25℃时,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后,溶液的pH=7,
则溶液中c(CH3COO-) + c(CH3COOH)= ,m与n的大小关系是m n(填“ >”“=”或“<”)。
(5)25℃时,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的pH=7 ,则NH3·H2O的电离常数Ka= 。
(1)①②⑥⑤④③
(2)5.9×10-10
(3)酸性 c(Na+) + c(H+) = c(CH3COO-) + c(OH-)。
(4)m/2 mol/L >
(5)1.7×10-5mol/L
(2)5.9×10-10
(3)酸性 c(Na+) + c(H+) = c(CH3COO-) + c(OH-)。
(4)m/2 mol/L >
(5)1.7×10-5mol/L
试题分析:(1)①HCl是一元强酸, ②CH3OOH是一元弱酸, ③Ba(OH)2是二元强碱,④Na 2CO3是强碱弱酸盐,⑤KCl是强酸强碱盐,⑥NH4Cl是强酸弱碱盐。酸性:强酸大于弱酸大于强酸弱碱盐;碱性:碱的大于强碱弱酸盐的。所以这几种溶液pH由小到大的顺序为①②⑥⑤④③.
(2)KHAc
 CH3COO-+H+,
CH3COO-+H+,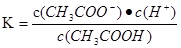 ,该温度下CH3COONa的水解平衡为CH3COO-+H2O
,该温度下CH3COONa的水解平衡为CH3COO-+H2O CH3COOH+OH-。
CH3COOH+OH-。水解平衡常数
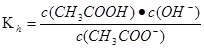

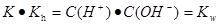
所以
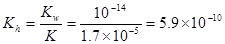 。(3)25℃时,pH=3的醋酸,c(H+)=10-3mol/L, pH=11的氢氧化钠溶液,c(H+)=10-11mol/L,则c(OH-)=Kw÷c(H+)=10-14÷10-11=10-3mol/L.两种溶液中的离子浓度相等。当等体积混合后,电离的部分巧合完全中和。但由于醋酸为弱酸。还有大量为电离的醋酸分子存在,会继续电离产生H+和CH3COO-。所以溶液呈酸性。在溶液中存在电荷守恒。c(Na+) + c(H+) = c(CH3COO-) + c(OH-)。(4)由于溶液为等体积混合,所以溶液中c(CH3COO-) + c(CH3COOH)=m/2mol/L。因为酸是弱酸,碱是强碱,若等物质的量混合,这恰好生成CH3COONa。溶液由于CH3COO-的水解二显碱性。为了使溶液显中性,酸必须稍微过量一些,来抵消醋酸根离子水解的碱性。所以m与n的大小关系是m>n. (5)25℃时,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的pH=7 ,说明醋酸与一水合氨的强弱程度相同。也就是电离程度相等。由于醋酸的电离平衡常数为Ka=1.7×10-5mol/L所以NH3·H2O的电离常数Ka=1.7×10-5mol/L。
。(3)25℃时,pH=3的醋酸,c(H+)=10-3mol/L, pH=11的氢氧化钠溶液,c(H+)=10-11mol/L,则c(OH-)=Kw÷c(H+)=10-14÷10-11=10-3mol/L.两种溶液中的离子浓度相等。当等体积混合后,电离的部分巧合完全中和。但由于醋酸为弱酸。还有大量为电离的醋酸分子存在,会继续电离产生H+和CH3COO-。所以溶液呈酸性。在溶液中存在电荷守恒。c(Na+) + c(H+) = c(CH3COO-) + c(OH-)。(4)由于溶液为等体积混合,所以溶液中c(CH3COO-) + c(CH3COOH)=m/2mol/L。因为酸是弱酸,碱是强碱,若等物质的量混合,这恰好生成CH3COONa。溶液由于CH3COO-的水解二显碱性。为了使溶液显中性,酸必须稍微过量一些,来抵消醋酸根离子水解的碱性。所以m与n的大小关系是m>n. (5)25℃时,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的pH=7 ,说明醋酸与一水合氨的强弱程度相同。也就是电离程度相等。由于醋酸的电离平衡常数为Ka=1.7×10-5mol/L所以NH3·H2O的电离常数Ka=1.7×10-5mol/L。
练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
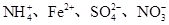
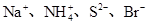
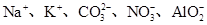
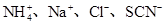
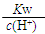 =0.1 mol·L-1的溶液:Na+、K+、CO32-、NO3—
=0.1 mol·L-1的溶液:Na+、K+、CO32-、NO3—