题目内容
【题目】某学习小组探究潮湿的Cl2与Na2CO3反应的产物,进行如下实验根据设计要求回答:
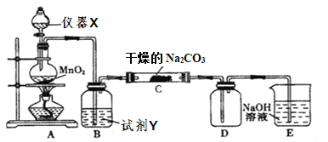
⑴X仪器名称是____________。
⑵装置A中发生反应的离子方程式:____________。
⑶B装置中试剂Y的作用是____________。
⑷下列有关该实验的说法中,不正确的是____________。
A.如图组装好实验仪器后,要先检查装置气密性,后添加药品
B.E装置的作用是吸收尾气防止污染空气
C.装置C中Cl2与Na2CO3以等物质的量反应,且生成的气体产物仅为Cl2O,可知反应方程式为2Cl2+2Na2CO3+H2O=2NaHCO3+2NaCl+Cl2O↑
D.试剂Y是浓硫酸,目的是干燥氯气
⑸设计实验方案验证C中生成的固体中存在![]() ____________。
____________。
【答案】分液漏斗 MnO2+ 4H++ 2Cl- ![]() Mn2++ Cl2↑+ 2H2O 除去氯气中混有的HCl D 取少量反应后的固体于试管中,加水溶解,滴加足量氯化钡溶液,静置一段时间后,再向试管中滴加NaOH溶液,若变浑浊,说明固体中含有碳酸氢根离子
Mn2++ Cl2↑+ 2H2O 除去氯气中混有的HCl D 取少量反应后的固体于试管中,加水溶解,滴加足量氯化钡溶液,静置一段时间后,再向试管中滴加NaOH溶液,若变浑浊,说明固体中含有碳酸氢根离子
【解析】
二氧化锰和浓盐酸反应生成氯化锰、氯气和水,用饱和食盐水吸收挥发出的HCl,湿润的氯气和碳酸钠反应生成Cl2O,根据得失电子守恒和原子守恒关系书写化学方程式,尾气用NaOH溶液吸收。
⑴根据图中仪器的特点,X仪器名称是分液漏斗;故答案为:分液漏斗。
⑵装置A中是二氧化锰和浓盐酸反应生成氯化锰、氯气和水,反应的离子方程式:MnO2+ 4H++ 2Cl- ![]() Mn2++ Cl2↑+ 2H2O;故答案为:MnO2+ 4H++ 2Cl-
Mn2++ Cl2↑+ 2H2O;故答案为:MnO2+ 4H++ 2Cl- ![]() Mn2++ Cl2↑+ 2H2O。
Mn2++ Cl2↑+ 2H2O。
⑶B装置中试剂Y主要的作用是除去氯气中混有的HCl;故答案为:除去氯气中混有的HCl。
⑷A.制取气体的实验中,先如图组装好实验仪器后,要先检查装置气密性,后添加药品,故A正确;
B.氯气有毒,会污染环境,因此E装置的作用是吸收尾气防止污染空气,故B正确;
C.装置C中Cl2与Na2CO3以等物质的量反应,且生成的气体产物仅为Cl2O,根据得失电子守恒和原子守恒,反应的化学方程式为2Cl2+2Na2CO3+H2O=2NaHCO3+2NaCl+ Cl2O↑,故C正确;
D.与碳酸钠反应需要潮湿的氯气,因此试剂Y不能是浓硫酸,试剂Y应为饱和食盐水,故D错误;
综上所述,答案为D。
⑸设计实验方案验证C中生成的固体中存在![]() :取少量反应后的固体于试管中,加水溶解,滴加足量氯化钡溶液,静置一段时间后,再向试管中滴加NaOH溶液,若变浑浊,说明固体中含有碳酸氢根离子;故答案为:取少量反应后的固体于试管中,加水溶解,滴加足量氯化钡溶液,静置一段时间后,再向试管中滴加NaOH溶液,若变浑浊,说明固体中含有碳酸氢根离子。
:取少量反应后的固体于试管中,加水溶解,滴加足量氯化钡溶液,静置一段时间后,再向试管中滴加NaOH溶液,若变浑浊,说明固体中含有碳酸氢根离子;故答案为:取少量反应后的固体于试管中,加水溶解,滴加足量氯化钡溶液,静置一段时间后,再向试管中滴加NaOH溶液,若变浑浊,说明固体中含有碳酸氢根离子。

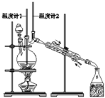
【题目】已知:CH3CH2CH2CH2OH![]() CH3CH2CH2CHO;利用如图装置用正丁醇合成正丁醛相关数据如表:
CH3CH2CH2CHO;利用如图装置用正丁醇合成正丁醛相关数据如表:
物质 | 沸点/℃ | 密度 / gcm-3 | 水中溶解性 |
|
正丁醇 | 117.2 | 0.8109 | 微溶 | |
正丁醛 | 75.7 | 0.8017 | 微溶 |
下列说法中,不正确的是
A.为防止产物进一步氧化,应将酸化的Na2Cr2O7溶液逐滴加入正丁醇中
B.当温度计1示数为90~95℃,温度计2示数在76℃左右时,收集产物
C.反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出
D.向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇