题目内容
2.对于反应:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,已知158g KMnO4反应生成了16g O2,则固体残余物的质量是( )| A. | 16g | B. | 32g | C. | 126g | D. | 142g |
分析 质量守恒定律:在化学反应中,参加反应的反应物的总质量等于生成物的总质量,据此解答即可.
解答 解:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,已知158g KMnO4反应生成了16g O2,则剩余固体质量为:158-16=142g,故选D.
点评 本题主要考查的是质量守恒定律定律的应用,此反应中只有氧气一种气体,故减去氧气的质量即为剩余固体的质量,难度不大.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
12.下列叙述中正确的是( )
| A. | 14C可用于文物的年代鉴定,14C与13C互为同素异形体 | |
| B. | 最外层电子数为2的元素一定是金属元素 | |
| C. | 过渡元素一定是金属元素 | |
| D. | 同一周期中的第ⅡA族和第ⅢA族元素的原子序数差一定为1或11 |
13.1998年山西朔州发生假酒案,假酒中严重超标的有毒成份主要是( )
| A. | 丙三醇 | B. | 甲醛 | C. | 乙二醇 | D. | 甲醇 |
10.乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明不正确的是( )
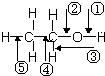

| A. | 和金属钠作用时,键①断裂 | |
| B. | 和浓硫酸共热至170℃时,键②和⑤断裂 | |
| C. | 和浓氢溴酸共热时,键②和③断裂 | |
| D. | .在铜催化下和氧气反应时,键①和③断裂 |
7.下列说法正确的是( )
| A. | 二氧化硅可以用来制造光导纤维 | |
| B. | 工艺师利用盐酸刻蚀石英制作艺术品 | |
| C. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| D. | 粗硅制单晶硅不涉及氧化还原反应 |
14.元素X的原子核外M电子层上有3个电子,元素Y2-的离子核外有18个电子,则这两种元素可形成的化合物为( )
| A. | XY2 | B. | X2Y3 | C. | X3Y2 | D. | X2Y |
11.下表是不同温度下水的离子积的数据:
试回答以下问题:
(1)若25<t1<t2,则a>1×10-14(填“>”、“<”或“=”),做此判断的理由是温度升高,水的电离程度增大,离子积增大.
(2)25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol•L-1,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+):c(OH-)=1 000:1.
(3)在t2温度下测得某溶液pH=7,该溶液显碱(填“酸”、“碱”或“中”)性,将此温度下pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合,若所得混合液pH=2,则a:b=9:11.
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积 | 1×10-14 | a | 1×10-12 |
(1)若25<t1<t2,则a>1×10-14(填“>”、“<”或“=”),做此判断的理由是温度升高,水的电离程度增大,离子积增大.
(2)25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol•L-1,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+):c(OH-)=1 000:1.
(3)在t2温度下测得某溶液pH=7,该溶液显碱(填“酸”、“碱”或“中”)性,将此温度下pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合,若所得混合液pH=2,则a:b=9:11.