题目内容
19.水溶液中能大量共存的一组离子是( )| A. | NH4+、Ba2+、Br-、CO32- | B. | K+、Na+、SO42-、MnO4- | ||
| C. | Na+、H+、NO3-、HCO3- | D. | Cl-、NO3-、Fe2+、H+ |
分析 A.钡离子与碳酸根离子反应生成碳酸钡沉淀;
B.四种离子之间不发生反应;
C.氢离子与碳酸氢根离子反应;
D.硝酸根离子在酸性条件下具有氧化性,能够氧化亚铁离子.
解答 解:A.Ba2+、CO32-之间反应生成碳酸钡沉淀,在溶液中不能大量共存,故A错误;
B.K+、Na+、SO42-、MnO4-之间不反应,在溶液中能够大量共存,故B正确;
C.H+、HCO3-之间发生反应,在溶液中不能大量共存,故C错误;
D.NO3-、Fe2+、H+之间发生氧化还原反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的正误判断,为中等难度的试题,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
11.下列单质或化合物的性质描述正确的是( )
| A. | NaHC03水溶液显碱性,溶液中阳离子电荷总数小于阴离子电荷总数 | |
| B. | SiO2不跟碱反应,但可与氢氟酸反应 | |
| C. | NO2难液化,易溶于水并跟水反应 | |
| D. | Fe3O4能与浓盐酸反应生成FeCl2和FeCl3 |
7.X、Y、Z是分别位于第2、3周期的元素,原子序数依次递增.X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半.下列说法正确的是( )
| A. | 工业上制取Y的单质常用还原剂还原Y的氧化物 | |
| B. | Z的最高价氧化物能与水反应生成相应的酸 | |
| C. | 室温下,X的最高价氧化物的水溶液的pH>7 | |
| D. | Y单质在一定条件下可以与氧化铁发生置换反应 |
4.高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理为:2Fe(OH)3+3KClO+4KOH═2K2FeO4+3KCl+5H2O,下列说法正确的是( )
| A. | ClO-做还原剂 | |
| B. | 制备1molK2FeO4时转移3mol 电子 | |
| C. | 高铁酸钾中铁的化合价为+7 | |
| D. | Fe(OH)3在反应中被还原,发生还原反应 |
11.NH3及其盐都是重要的化工原料.
(1)用NH4Cl和Ca(OH)2制备NH3的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;该反应发生、气体收集和尾气处理装置如图1依次为BDE;
(2)按如图2装置进行NH3性质实验.先打开旋塞1,B瓶中的现象是产生白色的烟,稳定后,关闭旋塞1.再打开旋塞2,B瓶中的现象是烧杯中的石蕊溶液会倒吸入B瓶,且溶液变为红色;
(3)写出NH4Cl溶液水解的离子方程式NH4++H2O?NH3•H2O+H+;
设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响.
限选试剂与仪器:固体NH4Cl、蒸馏水、250mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、pH计、温度计、恒温水浴槽(可调控温度)
①实验目的:探究温度对溶液中NH4Cl水解程度的影响;
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中“V(溶液)”表示所配制溶液的体积).
③按实验序号1所拟数据进行实验,若读取的待测物理量的数值为X,则NH4Cl水解反应的平衡转化率为$\frac{1{0}^{-X}×0.25×53.5}{m}$(只列出算式,忽略水自身电离的影响).

(1)用NH4Cl和Ca(OH)2制备NH3的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;该反应发生、气体收集和尾气处理装置如图1依次为BDE;
(2)按如图2装置进行NH3性质实验.先打开旋塞1,B瓶中的现象是产生白色的烟,稳定后,关闭旋塞1.再打开旋塞2,B瓶中的现象是烧杯中的石蕊溶液会倒吸入B瓶,且溶液变为红色;
(3)写出NH4Cl溶液水解的离子方程式NH4++H2O?NH3•H2O+H+;
设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响.
限选试剂与仪器:固体NH4Cl、蒸馏水、250mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、pH计、温度计、恒温水浴槽(可调控温度)
①实验目的:探究温度对溶液中NH4Cl水解程度的影响;
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中“V(溶液)”表示所配制溶液的体积).
| 物理量 实验序号 | V(溶液)/mL | NH4Cl质量/g | 温度/℃ | pH | … |
| 1 | 250 | m | T1 | X | … |
| 2 | 250 | m | T2 | Y | … |

5.为探讨催化剂的比表面积大小、温度高低等外部因素对反应3A2(g)+B(g)?2M(g)的反应速率的影响情况,某同学设计了三组恒压实验,部分实验条件如下表所示,下列有关数据的选择中错误的是( )
| 实验编号 | T/K | A的初始浓度/mol•L-1 | B的初始浓度/mol•L-1 | 催化剂的比表面积/m2•g-1 |
| Ⅰ | 200 | 0.40 | 0.60 | 82 |
| Ⅱ | T | 0.40 | 0.60 | 124 |
| Ⅲ | 220 | c1 | c2 | S |
| A. | T=200 | B. | S=100 | C. | c1=0.40 | D. | c2=0.60 |
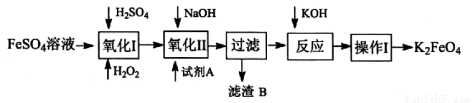
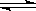 Fe(OH)3(胶体)+ KOH + 。
Fe(OH)3(胶体)+ KOH + 。
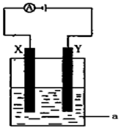 (1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是C;
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是C;