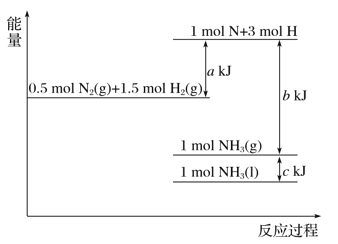
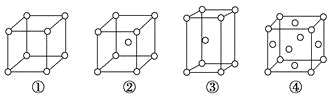
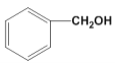
题目内容
【题目】在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:
Ni(s)+4CO(g)![]() Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法不正确的是
A. 上述生成Ni(CO)4(g)的反应为放热反应
B. 在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,则此时V(正)>V(逆)
C. 25℃时反应Ni(CO)4(g)![]() Ni(s)+4CO(g)的平衡常数为2×10-5 (mol·L-1)3
Ni(s)+4CO(g)的平衡常数为2×10-5 (mol·L-1)3
D. 80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度2 mol/L。
【答案】B
【解析】A.由表中数据可知,温度越高平衡常数越小,说明升高温度平衡向逆反应移动,升高温度平衡向吸热反应移动,故正反应为放热反应,A正确;B.浓度商Qc=0.5/0.54=8,大于80℃平衡常数2,故反应进行方向逆反应进行,故v(正)<v(逆),B错误;C. 25℃时反应Ni(s)+4CO(g)Ni(CO)4(g)的平衡常数为5×104,相同温度下,对于同一可逆反应的正、逆反应平衡常数互为倒数,故25°C时反应Ni(CO)4(g)Ni(s)+4CO(g)的平衡常数为1/5×104=2×10-5,C正确;D. 80℃达到平衡时,测得n(CO)=0.3mol,c(CO)=0.3mol/0.3L=1mol/L,故c[Ni(CO)4]=Kc4(CO)=2×14mol/L=2mol/L,D正确;答案选B。

【题目】将0.2molL-1的的KI溶液和0.05 molL-1Fe2(SO4)3溶液等体枳混合充分反应后,取混合液分别完成下列实验,能说明溶液中存在化学平衡2Fe3++2I-![]() 2 Fe2++I2的组合是
2 Fe2++I2的组合是
实验编号 | 实验操作 | 实验现象 |
① | 滴入KSCN溶液 | 溶液变红色 |
② | 滴入AgNO3溶液 | 有黄色沉淀生成 |
③ | 滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀生成 |
④ | 滴入淀粉溶液 | 溶液变蓝色 |
A. ①和② B. ②和③ C. ③和④ D. ①