题目内容
【题目】由S、Cl及Fe、Co、Ni等过渡元素组成的新型材料有着广泛的用途,回答下列问题:
(1)钴元素基态原子的电子排布式为_______,P、S、C1的第一电离能由大到小顺序为________。
(2)SCl2分子中的中心原子杂化轨道类型是_______,该分子空间构型为________。
(3)Fe、Co、Ni等过渡元素易与CO形成配合物,化学式遵循18电子规则:中心原子的价电子数加上配体提供的电子数之和等于18,如Ni与CO形成配合物化学式为Ni(CO)4,则Fe与CO形成配合物化学式为_______。Ni(CO)4中σ键与π键个数比为______,已知:Ni(CO)4熔点-19.3℃,沸点43℃,则Ni(CO)4为_______晶体。
(4)已知NiO的晶体结构如图1所示。
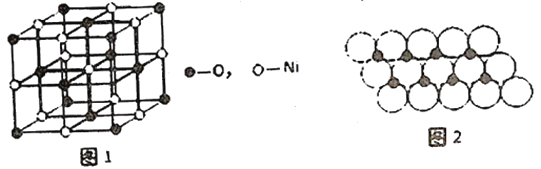
①NiO的晶体结构可描述为:氧原子位于面心和顶点,氧原子可形成正八面体空隙和正四面体空隙,镍原子填充在氧原子形成的空隙中。则NiO晶体中镍原子填充在氧原子形成的____体空隙中。
②已知MgO与NiO的晶体结构相同,其中Mg2+和Ni2+的离子半径分别为66pm和69pm。则熔点:MgO____NiO(填“>”、“<”或“=”),理由是_______________。
③一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充O2-形成的正三角形空隙中(如图2),己知O2-的半径为am,每平方米面积上分散的NiO的质量为______g。(用a、NA表示)
【答案】 1s22s22p63s23p63d74s2或[Ar] 3d74s2 Cl> P > S sp3 V 形 Fe(CO)5 1︰1 分子 正八面 > Mg2+半径比 Ni2+小, MgO 的晶格能比 NiO 大 ![]()
【解析】(1)钴元素是第27号元素,位于第四周期第ⅧB族,基态原子的电子排布式为1s22s22p63s23p63d74s2或[Ar] 3d74s2;同周期元素第一电离能从左到右有增大的趋势,第一电离能排序时,P元素电子排布有半充满结构,第一电离能较高,高于S 元素而低于Cl 元素,故第一电离能大小顺序为Cl> P > S。(2)![]() 做配体时有2个孤对电子,则可提供的电子数为2,
做配体时有2个孤对电子,则可提供的电子数为2,![]() 的价电子是
的价电子是![]() ,一共有8个,遵循18电子规则,则
,一共有8个,遵循18电子规则,则![]() 与
与![]() 形成配合物化学式为
形成配合物化学式为![]() 。
。![]() 中
中![]() 原子杂化轨道数为
原子杂化轨道数为![]() ,采取
,采取![]() 杂化方式,该分子构型为V形。(3)每个
杂化方式,该分子构型为V形。(3)每个![]() 分子内含有1个
分子内含有1个![]() 键和2个
键和2个![]() 键,而每个
键,而每个![]() 分子同时又通过1个
分子同时又通过1个![]() 配位键与
配位键与![]() 原子连接,所以
原子连接,所以![]() 键和
键和![]() 键之比为
键之比为![]() 。
。![]() 是由配位键形成的化合物,配位键属于共价键的一种,所以该物质是分子晶体。(4)①由图可知,氧原子形成的正四面体空隙中不含镍原子,中间是空的,形成的正八面体空隙中含有一个镍原子,则该晶体中镍原子填充在氧原子形成的正八面体空隙中。②晶体结构相同时,离子半径越小离子键强度越高,
是由配位键形成的化合物,配位键属于共价键的一种,所以该物质是分子晶体。(4)①由图可知,氧原子形成的正四面体空隙中不含镍原子,中间是空的,形成的正八面体空隙中含有一个镍原子,则该晶体中镍原子填充在氧原子形成的正八面体空隙中。②晶体结构相同时,离子半径越小离子键强度越高,![]() 半径比
半径比![]() 小,
小,![]() 的晶格能比
的晶格能比![]() 大,故熔点
大,故熔点![]() 。
。
③图中的单分子层可以如图画出一维重复单元:
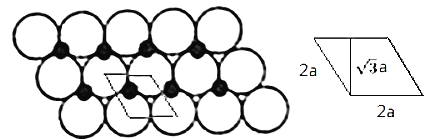
重复单元呈平行四边形,是相邻四个![]() 原子球中心的连线,每个重复单元包含1个
原子球中心的连线,每个重复单元包含1个![]() 原子和1个
原子和1个![]() 原子,
原子,![]() 相对分子质量为75。重复单元所占的平行四边形面积:
相对分子质量为75。重复单元所占的平行四边形面积:![]() ,则1平方米上该晶体质量为:
,则1平方米上该晶体质量为:![]() ,即。
,即。![]()

【题目】研究氮的氧化物、碳的氧化物等大气污染物的处理具有重要意义。
I. 已知:①N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-1 ②CO的燃烧热△H= - 283 kJ·mol-1
(1)汽车排气管内安装的催化转化器,可使尾气中主要污染物(NO和CO)转化为无毒的大气循环物质,该反应的热化学方程式为_________________________________________________。
(2)一定温度下,在恒容密闭容器中充入1 molNO和2 molCO进行该反应,下列能判断反应达到化学平衡状态的是_______。
①单位时间内消耗a mo1 CO的同时生成2a mol NO
②混合气体的平均相对分子质量不再改变
③混合气体中NO和CO的物质的量之比保持不变
④混合气体的密度不再改变
II. 臭氧是理想的烟气脱硝试剂,其脱硝反应为2NO2(g)+O3(g)![]() N2O5(g)+O2(g),向甲、乙两个体积都为1.0 L的恒容密闭容器中分别充入2.0 mol NO2和1.0 mol O3,分别在T1、T2温度下,经过一段时间后达到平衡。反应过程中n(O2)随时间(t)变化情况见下表:
N2O5(g)+O2(g),向甲、乙两个体积都为1.0 L的恒容密闭容器中分别充入2.0 mol NO2和1.0 mol O3,分别在T1、T2温度下,经过一段时间后达到平衡。反应过程中n(O2)随时间(t)变化情况见下表:
t/s | 0 | 3 | 6 | 12 | 24 | 36 |
甲容器(T1)n(O2)/mol | 0 | 0.36 | 0.60 | 0.80 | 0.80 | 0.80 |
乙容器(T2)n(O2)/mol | 0 | 0.30 | 0.50 | 0.70 | 0.85 | 0.85 |
(3)T1___T2(填>、<或=,下同),该反应ΔH___0 。简述理由________________________________。
(4)甲容器中,0~3s内的平均反应速率v(NO2)=______________________。
(5)甲容器中NO2平衡转化率为________,T1时该反应的平衡常数为_______________________。
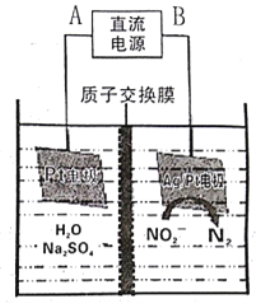
III. 将NO2(g)转化为N2O4(g)

(6)石墨I为______极(选填正、负),Y化学式为_________。
(7)II电极反应式为_________________________________________。