题目内容
【题目】现有七种元素,其中A、B、C为短周期主族元素,D、E为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
A元素的核外电子数和电子层数相等 |
B元素原子的核外p电子数比s电子数少1 |
C元素的第一至第四电离能如下: I1=738kJ·mol-1 I2=1451kJ·mol-1 I3=7733kJ·mol-1 I4=10540kJ·mol-1 |
D是前四周期中电负性最小的元素 |
E在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式:___。
(2)B元素基态原子中能量最高的电子的电子云在空间有___个伸展方向,原子轨道呈___形。
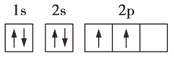
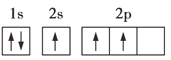
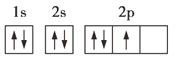
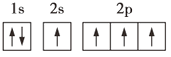
(3)某同学根据上述信息,推断C基态原子的电子排布图为![]() ,该同学所画的电子排布图违背了___。
,该同学所画的电子排布图违背了___。
(4)E位于第__族、__区,该元素原子的核外电子排布式为___。
(5)检验D元素的方法是___,请用原子结构的知识解释产生此现象的原因:__。
【答案】![]() 3 哑铃 泡利原理 ⅦB d 1s22s22p63s23p63d54s2 焰色反应 当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子。电子从较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量
3 哑铃 泡利原理 ⅦB d 1s22s22p63s23p63d54s2 焰色反应 当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子。电子从较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量
【解析】
A、B、C为短周期主族元素,D、E为第四周期元素,它们的原子序数依次增大,A元素的核外电子数和电子层数相等,则A为H元素;B元素原子的核外p电子数比s电子数少1,核外电子排布式为1s22s22p3,故B为N元素;由C原子的第一至第四电离能数据可知,第三电离能剧增,故C表现+2价,处于ⅡA族,原子序数大于N元素,故C为Mg元素;D是前四周期中电负性最小的元素,D为第四周期元素,故D为K元素;E在第四周期周期表的第7列,E为Mn元素。
(1) NH5为离子化合物,是由NH4+与H两种粒构成,电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(2) B为N元素,核外电子排布式为1s22s22p3,基态原子中能量最高的电子处于2p能级,有3个电子,其电子云在空间有3个方向,原子轨道呈哑铃形,故答案为:3,哑铃;
(3)某同学根据上述信息,推断C基态原子的核外电子排布为![]() ,该同学所画的电子排布图中3s能级中2个电子自旋方向相同,违背了泡利原理,故答案为:泡利原理;
,该同学所画的电子排布图中3s能级中2个电子自旋方向相同,违背了泡利原理,故答案为:泡利原理;
(4) G为Mn元素,核外电子排布式为1s22s22p63s23p63d54s2,位于第四周期第ⅦB族,最后填充的为d电子,为d区元素,故答案为:ⅦB;d; 1s22s22p63s23p63d54s2;
(5) 检验K元素的实验方法是:焰色反应;产生焰色反应的原因是:当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子。电子从较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量;故答案为:焰色反应;当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子。电子从较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量。

【题目】下列实验方案、现象、得出的结论均正确的是( )
选项 | 实验及现象 | 结论 |
A | 用酸度计测定 |
|
B | 向待测液中依次滴入氯水和 | 待测溶液中含有 |
C | 向酸化的 | 证明 |
D | 其他条件相同,测定等浓度的 | td style="width:153.75pt; border-top-style:solid; border-top-width:0.75pt; border-left-style:solid; border-left-width:0.75pt; padding:3.38pt 5.62pt; vertical-align:middle">
A.AB.BC.CD.D