题目内容
X、Y、Z是三种短周期的主族元素,在周期表的位置如图,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )
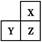

| A.原子半径:Y>Z>X |
| B.气态氢化物的热稳定性:X<Z |
| C.Y和Z的最高价氧化物对应水化物均为强酸 |
| D.若Z的最高正价为+m,则X的最高正价也一定为+m |
A
根据X原子的最外层电子数是其次外层电子数的3倍,可知X元素为O元素,Z元素为S元素,Y元素为P元素。根据同周期从左到右原子半径逐渐减小,同主族从上到下原子半径逐渐增大可得A对;气态氢化物的热稳定性比较是比较非金属性的强弱,同主族从上到下元素的非金属性减弱,所以H2S稳定性比H2O小,B错;Y的最高价氧化物对应水化物为磷酸是中强酸,Z对应的是H2SO4,是强酸,C错;S的最高价为+6价,而O不是,D错。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
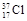 、
、 互为同位素,
互为同位素,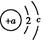 表示
表示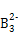 、A2
、A2