题目内容
1.如图是苯和溴的取代反应的实验装置图,其中A为具有支管的试管改制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量的铁屑粉.填写下列空白:(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应.写出A中发生反应的化学方程式(有机物写结构简式)C6H6+Br2$\stackrel{FeBr_{3}}{→}$C6H5Br+HBr
(2)试管C中苯的作用是吸收Br2蒸气、苯蒸气.反应开始后,观察E试管,看到的现象是E管中出现浅黄色沉淀
(3)反应2min~3min后,在B中的氢氧化钠溶液里可观察到的现象是底层出现油状液体
(4)在上述整套装置中,具有防倒吸作用的仪器有F(填字母).
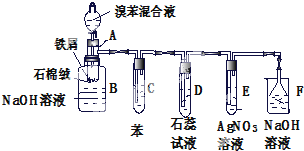
分析 根据实验装置图可知,液溴和苯的混合物滴加到有铁粉的石棉网上,液溴和苯在Fe作催化剂条件下能发生取代反应生成溴苯与HBr,溴和苯都是易挥发的物质,所以反应生成的溴苯及大部分未的反应苯和溴流入到下面的氢氧化钠溶液中,生成的溴化氢及挥发出的溴、苯通过C装置,苯和溴被吸收,溴化氢气体到D装置中能使石蕊变红,在E装置中溴化氢使硝酸银产生浅黄色沉淀,尾气用氢氧化钠吸收,由于溴化氢极易溶于水,所以F装置要用防止倒吸装置.
(1)Fe与溴反应生成溴化铁,苯和液溴在溴化铁作催化剂条件下能发生取代反应生成溴苯与HBr;
(2)溴苯中的溴易挥发,非极性分子的溶质易溶于非极性分子的溶剂,据此分析苯的作用;该反应中有溴化氢生成,溴化氢溶于水得到氢溴酸,氢溴酸能使石蕊试液变红色;氢溴酸能和硝酸银反应生成淡黄色沉淀溴化银;
(3)溴苯是有机物,不溶于氢氧化钠溶液,且密度大于氢氧化钠溶液;
(4)倒置的漏斗下口很大,具有缓冲作用,球形干燥管球形部分,空间大,两者都能防止溶液倒吸,该题具有防倒吸作用的仪器为倒置的漏斗.
解答 解:(1)Fe与溴反应生成溴化铁,苯和液溴在溴化铁作催化剂条件下能发生取代反应,苯环上的氢原子被溴原子所取代,生成溴苯与HBr,反应方程式为:2Fe+3Br2=2FeBr3,C6H6+Br2$\stackrel{FeBr_{3}}{→}$C6H5Br+HBr,
故答案为:C6H6+Br2$\stackrel{FeBr_{3}}{→}$C6H5Br+HBr;
(2)制取溴苯的原料溴、苯易挥发,溴、苯都是非极性分子,根据相似相溶原理知,溴易溶于苯,所以苯的作用是吸收溴蒸气、苯蒸气,该反应中有溴化氢生成,溴化氢溶于水得到氢溴酸,氢溴酸是酸性物质,能使石蕊试液变红色;氢溴酸能和硝酸银反应生成淡黄色沉淀溴化银,所以观察D和E两试管,看到的现象是D管中变红,E管中出现浅黄色沉淀,
故答案为:吸收Br2蒸气、苯蒸气;E管中出现浅黄色沉淀;
(3)溴苯是有机物,氢氧化钠溶液是无机物,所以溴苯和氢氧化钠溶液不互溶,且溴苯的密度大于水的密度,所以在B中的氢氧化钠溶液里可观察到的现象是底层出现油状液体,
故答案为:底层出现油状液体;
(4)当两端压力发生压力变化时,液体会产生倒吸现象,因为倒置的漏斗下口很大,液体上升很小的高度就有很大的体积,上升的液体的本身的压力即可低偿压力的不均衡.因此由于上部还有空气隔离,液体不会倒吸入上端的细管道,所以具有防倒吸作用的仪器有F,
故答案为:F.
点评 本题考查有机物实验制备,涉及溴苯的制取,侧重考查学生对装置与原理的分析评价,明确各个装置的作用及基本操作方法,题目难度中等.

 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
pH值控制可参考下列数据
| 物 质 | 开始沉淀时的pH值 | 完全沉淀时的pH值 |
| 氢氧化铁 | 2.7 | 3.7 |
| 氢氧化亚铁 | 7.6 | 9.6 |
| 氢氧化铜 | 5.2 | 6.4 |
(1)A物质可选用b(填字母).
a.稀H2SO4b.浓H2SO4/△c.浓FeCl3溶液 d.浓HNO3
(2)Ⅰ中加H2O2的目的将Fe2+氧化为Fe3+.
(3)Ⅱ中加Cu2(OH)2CO3的目的是中和过量的硫酸,调节溶液的pH,使Fe3+水解完全而沉淀;其优点是不引入新的杂质.
(4)Ⅲ加热煮沸时发生的化学反应的离子方程式为Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3H+.
(5)V中加H2SO4调节pH=1是为了抑制Cu2+的水解.
(6)V到Ⅵ的操作是蒸发浓缩,冷却结晶,过滤
(7)某工程师认为上述流程中所加的A物质并不理想,需作改进,其理由是会产生SO2,会对污染环境,硫酸的利用率低.如何改进可以向稀硫酸中不断通氧气(或者加H2O2)并加热.
 =BaSO4↓
=BaSO4↓ =CaCO3↓+CO
=CaCO3↓+CO +2H2O
+2H2O ;
;
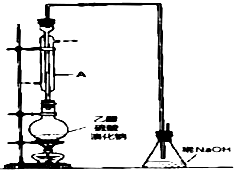 溴乙烷是一种重要的有机化工原料,其沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸、浓硫酸共热发生反应,该反应的化学方程式是CH3CH2OH+HBr$→_{△}^{浓硫酸}$CH3CH2Br+H2O
溴乙烷是一种重要的有机化工原料,其沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸、浓硫酸共热发生反应,该反应的化学方程式是CH3CH2OH+HBr$→_{△}^{浓硫酸}$CH3CH2Br+H2O