题目内容
14.取少量苹果汁,加入碘水,溶液变蓝,则苹果中含有( )| A. | 淀粉 | B. | 葡萄糖 | C. | 无机盐 | D. | 油脂 |
分析 淀粉遇碘变蓝色,据此分析.
解答 解:取少量苹果汁,加入碘水,溶液变蓝,淀粉遇碘变蓝色,说明苹果汁中含有淀粉,故选A.
点评 本题考查了淀粉的性质,应注意的是淀粉遇碘单质变蓝,而不是碘元素,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.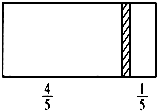 一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左边充入1molN2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置(左、右两侧温度相同),下列说法正确的是( )
一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左边充入1molN2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置(左、右两侧温度相同),下列说法正确的是( )
 一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左边充入1molN2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置(左、右两侧温度相同),下列说法正确的是( )
一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左边充入1molN2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置(左、右两侧温度相同),下列说法正确的是( )| A. | 右边CO与CO2分子数之比为1:3 | |
| B. | 右侧气体密度是相同条件下氢气密度的18倍 | |
| C. | 右侧CO的质量为1.75g | |
| D. | 若隔板处于距离右端$\frac{1}{6}$处,其他条件不变,则前后两次压强之比为25:24 |
2.下列反应是氧化还原反应的是( )
| A. | S2-+2H+═H2S↑ | B. | 2Fe3++Fe═3Fe2+ | ||
| C. | NH4Cl+NaOH═NH3•H2O+NaCl | D. | Ca(ClO)2+CO2+H2O═CaCO3+2HClO |
6.铜元素有质量数为63和65的两种天然同位素,它的近似相对原子质量是63.5,则同位素63Cu所占的质量百分比为( )
| A. | 20% | B. | 25% | C. | 74.4% | D. | 75% |
3.无机化合物可根据其组成和性质进行如下分类:
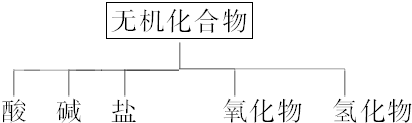
(1)
以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在上表②③⑥的后面.
(2)写出⑦转化为⑤的化学方程式:Na2O+CO2═Na2CO3.
(3)写出实验室由⑩制备O2的化学方程式:2H2O2$\frac{\underline{\;催化剂\;}}{\;}$ 2H2O+O2↑,.
(4)实验室制备⑦常用石灰石(或大理石)和稀盐酸反应,检验该气体的方法是将气体通入澄清的石灰水中,变浑浊,则说明该气体是CO2.

(1)
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ②H2S、HNO3、H2CO3、H2SO4 | ③NaOH、KOH ④Ba(OH)2 | ⑤Na2CO3 ⑥Na2CO3、Na2SO4、K2CO3、K2SO4、NaNO3、KNO3 | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(2)写出⑦转化为⑤的化学方程式:Na2O+CO2═Na2CO3.
(3)写出实验室由⑩制备O2的化学方程式:2H2O2$\frac{\underline{\;催化剂\;}}{\;}$ 2H2O+O2↑,.
(4)实验室制备⑦常用石灰石(或大理石)和稀盐酸反应,检验该气体的方法是将气体通入澄清的石灰水中,变浑浊,则说明该气体是CO2.
4.漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸(HClO2为弱酸)不稳定可分解,反应的离子方程式为:
5HClO2=4ClO2↑+H++Cl-+2H2O.向NaClO2溶液中滴加H2SO4,开始时HClO2分解反应反应缓慢,随后反应迅速,其原因是( )
5HClO2=4ClO2↑+H++Cl-+2H2O.向NaClO2溶液中滴加H2SO4,开始时HClO2分解反应反应缓慢,随后反应迅速,其原因是( )
| A. | 在酸性条件下,亚氯酸钠的氧化性增强 | |
| B. | 溶液中的Cl-起催化作用 | |
| C. | ClO2逸出,使反应的生成物浓度降低 | |
| D. | 溶液中的H+起催化作用 |
 A的晶胞如图所示,已知A相对原子质量为M,晶体密度ρg•cm-3,阿伏伽德罗常数为NA,A元素的原子半径为$\root{3}{\frac{2M}{ρ×{N}_{A}}}$×$\frac{\sqrt{3}}{4}$cm.(用M、ρ、NA表示,不用化简)
A的晶胞如图所示,已知A相对原子质量为M,晶体密度ρg•cm-3,阿伏伽德罗常数为NA,A元素的原子半径为$\root{3}{\frac{2M}{ρ×{N}_{A}}}$×$\frac{\sqrt{3}}{4}$cm.(用M、ρ、NA表示,不用化简)