题目内容
 50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
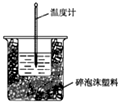
50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:(1)从实验装置上看,图中尚缺少的一种玻璃用品是
(2)烧杯间填满碎泡沫塑料的作用是
(3)大烧杯上如不盖硬纸板,求得的中和热△H的数值
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热△H的数值会
考点:中和热的测定
专题:实验题
分析:(1)根据量热计的构造来判断该装置的缺少仪器;
(2)中和热测定实验成败的关键是保温工作;
(3)大烧杯上如不盖硬纸板,会使一部分热量散失;
(4)根据弱电解质电离吸热分析.
(2)中和热测定实验成败的关键是保温工作;
(3)大烧杯上如不盖硬纸板,会使一部分热量散失;
(4)根据弱电解质电离吸热分析.
解答:
解:(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒,
故答案为:环形玻璃搅拌棒;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是减少实验过程中的热量损失,
故答案为:减少实验过程中的热量损失;
(3)大烧杯上如不盖硬纸板,会使一部分热量散失,求得的中和热数值将会减小,
故答案为:偏小;
(4)氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量偏小,求得的中和热数值将会减小,
故答案为:偏小.
故答案为:环形玻璃搅拌棒;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是减少实验过程中的热量损失,
故答案为:减少实验过程中的热量损失;
(3)大烧杯上如不盖硬纸板,会使一部分热量散失,求得的中和热数值将会减小,
故答案为:偏小;
(4)氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量偏小,求得的中和热数值将会减小,
故答案为:偏小.
点评:本题考查学生有关中和热的测定,题目难度中等,注意理解中和热的概念和测定原理是解题的关键.

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
已知H2S为弱酸,关于硫化氢水溶液,下列说法不正确的是( )
| A、常温下,pH小于7 |
| B、存在关系式:c(H+)=2c(S2-)+c(HS-)+c(OH-) |
| C、25℃时,由水电离产生的c(H+)>1×10-7mol?L-1 |
| D、向溶液中加入少量NaOH固体,c(S2-)增大 |
短周期元素M、W、X、Y、Z的原子序数依次增大,M元素的一种核素没有中子,且M、W、X、Y+、Z的最外层电子数与其电子层数的比值依次为1、2、3、4、2(不考虑零族元素).下列关于这些元素的叙述正确的是( )
| A、X分别和其它四种元素均可形成至少2种化合物 |
| B、M分别和W、X、Y、Z形成化合物,均显相同化合价 |
| C、M、X、Z三种元素组成的化合物含有离子键 |
| D、M、X、Y组成化合物和Y、Z组成化合物,其等物质的量浓度的水溶液中由水电离出的氢离子浓度相同 |
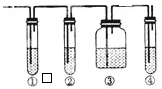 实验室中通常用浓硫酸使乙醇脱水制取少量乙烯,反应机理如为:CH3CH2OH→C2H4↑+H2O.实验中常因温度过高使乙醇与浓硫酸反应生成少量的二氧化硫气体.有人设计了如图的实验,以确定上述混合气体中是否含有乙烯和二氧化硫.
实验室中通常用浓硫酸使乙醇脱水制取少量乙烯,反应机理如为:CH3CH2OH→C2H4↑+H2O.实验中常因温度过高使乙醇与浓硫酸反应生成少量的二氧化硫气体.有人设计了如图的实验,以确定上述混合气体中是否含有乙烯和二氧化硫. 近年来,由于温室效应和资源短缺等问题,关于CO2和碳酸盐应用的研究受到人们的重视.某研究小组利用反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,制备CO2与H2 的混合气体,并进一步研究CO2与H2以不同的体积比混合时在合适条件下的反应产物应用.
近年来,由于温室效应和资源短缺等问题,关于CO2和碳酸盐应用的研究受到人们的重视.某研究小组利用反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,制备CO2与H2 的混合气体,并进一步研究CO2与H2以不同的体积比混合时在合适条件下的反应产物应用.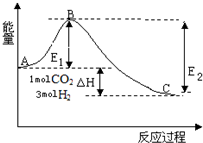 研究CO2的利用对促进低碳社会的构建具有重要的意义.
研究CO2的利用对促进低碳社会的构建具有重要的意义.