题目内容
下列说法正确的是
| A.放热反应在任意条件下都能自发进行 |
B.已知热化学方程式2A(g)+B(g) 2C(g)△H=-a kJ·mol-1(a>0)将2molA(g)和1molB(g)置于一密闭容器中充分反应后放出akJ的热量 2C(g)△H=-a kJ·mol-1(a>0)将2molA(g)和1molB(g)置于一密闭容器中充分反应后放出akJ的热量 |
| C.1mol·L-1的盐酸分别与1mol·L-1的氨水、1mol·L-1的NaOH溶液等体积混合,充分反应,后者比前者放出的热量多 |
| D.BaCl2溶液中加过量H2SO4,溶液中一定不存在Ba2+ |
C
A.放热但熵减的反应就不能在任意条件下都自发进行,A错误。
B.该反应是可逆反应,△H表示反应已经完成的量,即表示反应2molA(g)和1molB(g)时放出akJ的热量。而将2molA(g)和1molB(g)置于一密闭容器中充分反应,反应物是不能完全转化的,故放热小于akJ,B错误。
C.因氨水是弱碱,反应的同时发生电离,而电离吸热,故盐酸与氨水反应放出的热量少,C正确。
D. BaCl2溶液中加过量H2SO4,生成Ba SO4沉淀,存在沉淀溶解平衡,故溶液存在很少量的Ba2+中,D错误。
故选C
B.该反应是可逆反应,△H表示反应已经完成的量,即表示反应2molA(g)和1molB(g)时放出akJ的热量。而将2molA(g)和1molB(g)置于一密闭容器中充分反应,反应物是不能完全转化的,故放热小于akJ,B错误。
C.因氨水是弱碱,反应的同时发生电离,而电离吸热,故盐酸与氨水反应放出的热量少,C正确。
D. BaCl2溶液中加过量H2SO4,生成Ba SO4沉淀,存在沉淀溶解平衡,故溶液存在很少量的Ba2+中,D错误。
故选C

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目

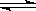 2SO3(g);ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是
2SO3(g);ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是 4NO (g)+ 6H2O(g)
4NO (g)+ 6H2O(g)
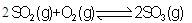
 (Q>0),若向一密闭容器中加入1molSO2和0.5molO2充分反应后,放出的热量为0.5QkJ
(Q>0),若向一密闭容器中加入1molSO2和0.5molO2充分反应后,放出的热量为0.5QkJ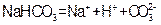

 、
、 时,
时, 完全燃烧生成气态水,放出
完全燃烧生成气态水,放出 热量,则氢气的燃烧热为241.8
热量,则氢气的燃烧热为241.8